【研究意义】魁蚶(Scapharca broughtonii)又称赤贝、血贝、大毛蛤,隶属软体动物门(Mollusca)、双壳纲(Bivalvia)、翼形亚纲(Pteriomorphia)、蚶目(Arcoida)、蚶科(Arcidae)、蚶属(Scapharca),是一种大型海洋底栖经济贝类,主要分布在太平洋西北部日本海、黄海、渤海及东海,分布区从近岸水深3~5 m到外海近60 m处。魁蚶成体个大体肥,肉质鲜美,经济价值很高。近年来,由于市场和出口大量需求,过度开发利用导致自然资源急剧下降[1],魁蚶已经不能满足国内外市场的需求。由于资源不足,魁蚶价格不断上涨,开展人工育苗、中间培育、底播和增殖放流等工作势在必行。【前人研究进展】国家通过设立魁蚶良种场、增殖放流,选育魁蚶品系,保护魁蚶自然资源,保持魁蚶种群特性,保证魁蚶品系质量[2]。近二十年,科研工作者对魁蚶的增养殖做了大量的工作,在魁蚶常温育苗和升温育苗过程中的一些技术环节进行了大量的研究,并取得显著的社会效益和经济效益。王子臣等[3]研究表明褐指藻可以使魁蚶的性腺发育较快;在饵料不足情况下以小球藻混合褐指藻效果最佳,单独饲以小球藻、褐指藻及人工配合饵料也取得较好的效果,以豆粉为主的饲料会导致性腺退化。王兴章等[4]认为水温对魁蚶孵化的影响是非常明显的,15℃和35℃均不能正常孵化,而25℃左右是魁蚶孵化的适宜温度。唐启升等[1]研究不同水温对魁蚶受精卵孵化的影响,结果表明受精卵孵化的适宜水温为22~27℃,在适宜范围内,温度越高,孵化时间越短;水温超过27℃,孵化率明显下降。陈觉民等[5]研究海水中某些化学因子对魁蚶幼虫、稚贝及成体的影响,认为魁蚶对盐度的适应范围随贝龄增大而减小,在不适盐度中,其忍受时间也随贝龄的增大而缩短;另外,盐度对稚贝的附着有一定影响。刘恩孚等[6]研究不同底播时间和苗种规格的魁蚶潜沙率差异性,认为底播时应选取潜沙速率快且潜沙率较为稳定的规格作为埋栖型贝类的底播规格,底播时间应根据当地海区潮汐情况确定。【本研究切入点】目前在魁蚶的育苗过程中,不同理化因子对魁蚶胚胎发育、幼虫生长和稚贝生长以及进行优良品系选育的研究大多集中在20世纪90年代,随着近年来魁蚶产业的不断发展,需要系统研究温度、盐度、饵料、密度等理化因子对魁蚶幼虫生长的影响,总结出一套完整的魁蚶人工育苗技术。【拟解决的关键问题】通过研究不同饵料投喂对魁蚶幼体生长的影响,为了解魁蚶幼虫生物学特性、更好地开展魁蚶育苗工作提供数据支持。
1 材料和方法 1.1 材料(1) 育苗设施:育苗场地位于日照市涛雒镇,包括动力抽水设备、沉淀过滤系统、水电气系统等,设施基本完备。
(2) 水质条件:海水水源符合国家渔业水质标准,育苗用水经二级过滤系统沉淀,再经入池管道口300目尼龙筛绢网滤出,经镜检无大型原生动物。
(3) 藻种:单胞藻饵料种类有金藻类(海大叉鞭金藻)、硅藻类(牟氏角毛藻)、绿藻类(小球藻);人工饵料为海洋酵母。在育苗场饵料车间培养金藻、角毛藻等生物饵料,海洋酵母(1×1010 cell/mL)、小球藻(2×1010 cell/mL)购自青岛洪邦生物技术有限公司,冷藏(0~4℃,保质期6个月)保存备用。
(4) 魁蚶亲贝及幼体:从涛雒镇小海村养殖厂购得,亲贝贝龄为3~4年,性腺发育良好,外观无破损。放置在育苗池中暂养15 d后待产,水温升至22℃催产,受精,采集一部分受精卵用于实验。
(5) 实验设备:75L的塑料大白桶(实验前两天用高锰酸钾和盐酸刷两遍,用过滤海水冲洗干净,晒干备用)。50 mL、100 mL、150 mL小烧杯各4个,碘酒1瓶,带有目微尺的显微镜一台(型号:奥林巴斯CX21),胶头吸管若干,血小球计数板1个,计数器1个。
1.2 方法室内进行实验,自然水温、自然光照、自然海水。24h微量充气。初始培育密度5个/mL。
(1) 实验设6个处理:金藻、角毛藻、海洋酵母、小球藻、金藻+角毛藻、金藻+海洋酵母,每处理4个重复。
(2) 投饵:每天投喂4次,6:00、12:00、18:00、24:00各投喂1次,每天监测金藻、角毛藻密度。
(3) 换水:每天上午换水1/2,使用筛绢网隔苗向外舀水,用水管将新水加入,水流尽量小,不要将桶底污物搅起。
(4) 吸底:每3~5d用细管虹吸桶底污物,用桶静置15 min左右将水和魁蚶幼虫倒回原桶,重复2~3次
(5) 实验期间不同饵料处理组和不同壳长魁蚶幼虫的投饵量和投饵方法如表 1所示。投饵量以满足魁蚶幼虫饱食为宜,饵料投喂量过少,不利于魁蚶幼虫的生长,过多则容易污染水质。
| 表 1 不同壳长魁蚶幼虫不同饵料每次饵料投喂量 Table 1 The per feeding amount of bait to different shell length and different bait of Scapharca broughtonii larvae |
(1) 饵料密度测定:每次投饵前将饵料摇匀,用胶头吸管吸取5 mL左右,在显微镜下用血小球计数板测定金藻和角毛藻的密度。
(2) 水温的测量:用水银温度计测定实验桶内的水温,每天测一次。
(3) 魁蚶D形幼虫壳长和壳高的测量:取样时,先用搅拌棒在桶中上下轻轻搅匀,然后用50mL的小烧杯在桶中的上、中、下3个位置取20 mL左右的水。取完样后,将少量的碘液加到烧杯中将幼虫麻醉,在带有目微尺的显微镜下测量壳长和壳高,重复测量30个幼虫的壳长和壳高。
1.3.2 生长指标测定实验开始测量初始壳长、壳高,实验结束后测量终壳长、终壳高,并计算特定生长率(SGR)。
SGR(%·d-1)=100×(LnL1-LnL0)/t,
其中:L1和L0分别为终壳长(终壳高)和初始壳长(初始壳高),t为实验天数。
1.3.3 数据统计分析各处理的数据进行单因素方差分析,当差异显著时(P<0.05),用Duncan’s检验法进行均值间多重比较,统计分析所用的软件为SPSS 19.0。
2 结果与分析 2.1 饵料密度及水温变化如表 2所示,实验期间金藻密度为5×105~9×105 cell/mL,角毛藻密度为5×105~10×105 cell/mL。实验期间桶内水温变化如表 3所示,水温保持在(20±1)℃。
| 表 2 金藻和角毛藻饵料密度(×105 cell/mL) Table 2 The density of Chrysophyta and Chaetoceros(×105 cell/mL) |
| 表 3 实验期间水温变化 Table 3 The changes of water temperature |
不同饵料投喂下魁蚶幼虫终壳长不同:金藻+海洋酵母处理组、金藻处理组终壳长都达到170μm以上,角毛藻处理组和小球藻处理组终壳长不足130 μm。
不同饵料投喂下魁蚶幼虫特定生长率大小依次为金藻+海洋酵母处理组>金藻处理组>海洋酵母处理组>金藻+角毛藻处理组>角毛藻处理组>小球藻处理组(表 4),各处理组间差异极显著(P<0.05)。
| 表 4 不同饵料投喂对魁蚶幼虫壳长生长的影响(平均值±标准误,n=6) Table 4 Effects of different bait feeding ways on the shell length growth of Scapharca broughtonii larvae(means±S.E., n=6) |
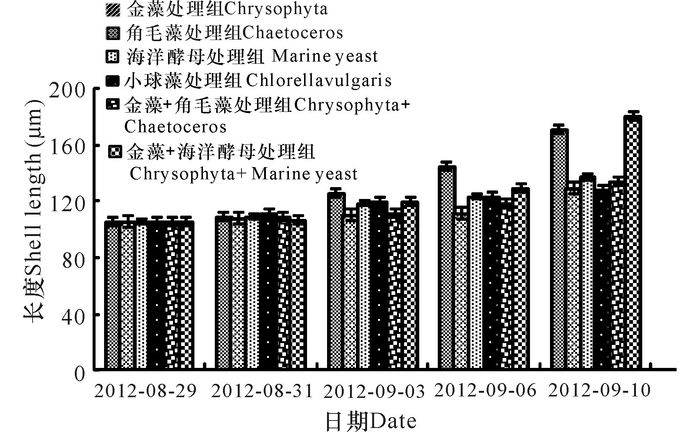
如图 1所示,实验开始后3d各处理组之间壳长差异并不明显,5 d后各处理组之间壳长差异明显,实验结束时壳长差异达到最大。金藻处理组壳长生长5 d后速度快而且比较平稳,金藻+海洋酵母处理组在8 d后速度明显增高。
|
图 1 不同饵料处理组下魁蚶幼虫的壳长生长 Fig.1 The shell long growth of S.broughtonii of different bait groups |
不同饵料投喂对魁蚶幼虫壳高生长影响的优劣程度为金藻+海洋酵母处理组>金藻处理组>海洋酵母处理组>金藻+角毛藻处理组>角毛藻处理组>小球藻处理组(表 5),各处理组间差异都极显著(P<0.05)。
| 表 5 不同饵料投喂对魁蚶幼虫壳高生长的影响(平均值±标准误,n=6) Table 5 Effects of different bait feeding ways on the shell high growth of Scapharca broughtonii larvae (means±S.E., n=6) |
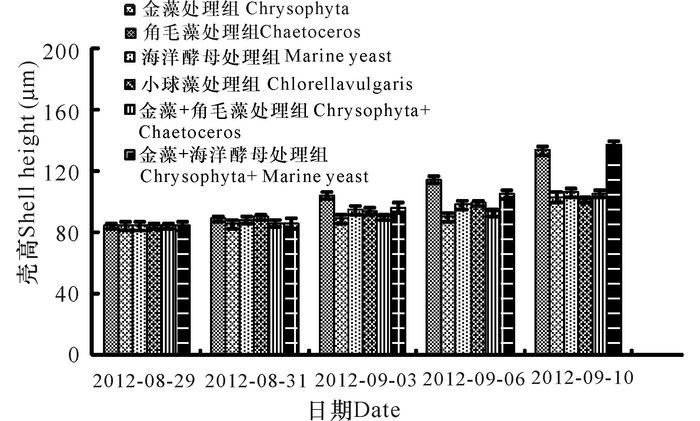
由图 2可见,金藻+海洋酵母处理组魁蚶幼虫壳高最长,其次依次为金藻处理组、海洋酵母处理组、金藻+角毛藻处理组、角毛藻处理组,小球藻处理组魁蚶幼虫壳高最短。
|
图 2 不同饵料处理下魁蚶幼虫的壳高生长 Fig.2 The shell high growth of S.broughtonii of different bait groups |
在魁蚶室内升温育苗过程中,饵料(藻类、人工饵料)是育苗成功与否的关键因子,生物饵料培育不好,就无法满足幼虫的生长营养需要,造成幼虫的畸形和死亡。作为贝类育苗的藻类有很多种,不同藻类效果不一样,混合投喂和单独投喂藻类对幼虫的生长会产生不同的效果,进而从多方面影响到贝类幼虫的生长、变态附着和成活[4]。
根据国内有关魁蚶幼体饵料方面的研究报道,等鞭金藻、叉鞭金藻均为幼虫培育阶段的良好饵料,在幼虫壳长130μm以上混投扁藻,更能促进幼虫生长[7]。D形幼虫期饵料以金藻为主,投饵量为3×104~4×104 cell/mL;眼点幼虫期,投饵量增加到6×104 cell/mL左右,能够满足幼虫正常发育需要[8]。幼体培育4~5 d以后,随着幼体长大可以添加小硅藻、扁藻等饵料[9]。
因D形幼虫只能滤食容易被消化的单胞藻类,所以在本实验中选取单胞藻做为研究对象,进行适合幼虫开口饵料的研究。由不同饵料投喂对魁蚶幼虫从D形幼虫到壳顶期生长影响的分析可以得出:若只投喂单一饵料,在魁蚶幼虫从D形幼虫发育到壳顶期这段时期内,金藻的投喂效果最好,因此在饵料不足的情况下,可以只选择投喂金藻来作为魁蚶幼虫的开口饵料,来保证幼虫生长发育的营养需要,这与其他贝类幼虫饵料得到的结果一致[10-14]。如沈伟良等[15]研究不同藻类对毛蚶浮游幼虫生长的影响,结果表明在3种不同单胞藻中,湛江球等鞭金藻的效果最好。孙虎山等[16]采用4种单胞藻来研究饵料密度对紫彩血蛤幼虫生长发育的影响,认为等边金藻的效果最好。贝类在不同的发育阶段对藻类有不同的需求,在D形幼虫发育到壳顶期这段时间,对饵料大小有明显的选择性。幼虫个体较小并且消化道未完全形成,所以在此阶段个体较小的金藻较为适合作为饵料进行投喂。根据实验结果,发现小球藻的效果最差,可能是由于小球藻具有较厚的细胞壁,加上幼虫的消化系统未发育完全,难以被幼虫消化[17]。单独投喂小球藻,虽能培育出稚贝,但幼虫生长速度较慢,成活率也很低[18]。
单一饵料存在着营养成分不够全面均衡等问题,而混合饵料则可以较为全面地提供幼虫生长发育所需的营养。在喂混合饵料投喂中,金藻+海洋酵母的效果最好,生物饵料加人工饵料的搭配效果明显。唐启升等[1]研究不同饵料对魁蚶幼虫生长发育的影响,表明叉鞭金藻+小球藻效果最好,人工饵料可以补充生物饵料营养成分的不足。有研究表明,两种消化速度不一的饵料混合可以使它们得到更充分地消化[17]。饵料多样性是影响幼体培养效果的重要因素,饵料种类越多,变态率越高,生长速度越快,不同饵料间的营养可以互补,多种饵料搭配能为幼体发育提供更全面的营养[18]。有关其他贝类幼虫发育过程中的幼体饵料也有报道,张善发等[19]研究了几种饵料对华贵栉孔扇贝浮游幼虫生长和成活的影响,试验结果表明投喂金藻和亚心形扁藻混合组生长速度最快,投喂金藻和酵母组次之,单独投喂亚心形扁藻时生长速度最差。何连金等[20]研究泥蚶幼虫和稚贝的适宜饵料,湛江叉鞭金藻、牟氏角毛藻、双突角毛藻、云微型藻是D型幼虫期的良好饵料,壳顶期幼虫及附着稚贝除上述种类外,青岛大扁藻的效果更好,使用混合饵料比单一饵料效果好。在本实验中,混合饵料金藻+海洋酵母比单一投喂金藻效果还要好,说明在魁蚶幼虫这一发育时期可以采取混合饵料投喂方式,但选择不同饵料搭配的时候要谨慎。金藻+角毛藻的效果不如单一投喂金藻和海洋酵母的好,说明在这一时期,不适合投喂角毛藻饵料。
| [1] |
唐启升, 邱显寅, 王俊, 等. 山东近海魁蚶资源增殖的研究[J]. 应用生态学报, 1994, 5(4): 396-402. TANG Q S, QIU Y S, WANG J, et al. Resource enhancement of arkshell (Scapharca(Anadara) broughionii) in Shandong off-shore waters[J]. Chinese Journal of Applied Ecology, 1994, 5(4): 396-402. |
| [2] |
张启刚, 王如才, 王兴章, 等. 魁蚶(Arca (Anadara) inflata Reeve)品系选育[J]. 现代渔业信息, 2007, 22(7): 25-26. ZHANG Q G, WANG R C, WANG X Z, et al. Selective breeding of strain of Arca (Anadara) inflata Reeve[J]. Modern Fisheries Information, 2007, 22(7): 25-26. |
| [3] |
王子臣, 张国范, 高悦勉, 等. 温度和饵料对魁蚶性腺发育的影响[J]. 大连水产学院学报, 1987(2): 1-10. WANG Z C, ZHANG G F, GAO Y M, et al. The effects of temperature and foods on the development of gonad of the blood cockle, Arca inflata[J]. Journal of Dalian Fisheries College, 1987(2): 1-10. |
| [4] |
王兴章, 邢信泽, 张启刚. 几种理化因子对魁蚶人工育苗的影响[J]. 齐鲁渔业, 2003, 20(2): 17-18. WANG X Z, XING X Z, ZHANG Q G. Effects of several physical and chemical factors on artificial breeding of Scapharca broughtonii[J]. Shandong Fisheries, 2003, 20(2): 17-18. |
| [5] |
陈觉民, 王恩明, 李何. 海水中某些化学因子对魁蚶幼虫、稚贝及成体的影响[J]. 海洋与湖沼, 1989, 20(1): 15-22. CHEN J M, WANG E M, LI H. The effects of some chemical factors on the larvae and adults of Scapharca broughtonii (Schrenek)[J]. Oceanologia et Limnoligia Scinica, 1989, 20(1): 15-22. |
| [6] |
刘恩孚, 刘广斌, 邱兆星, 等. 不同底播时间和苗种规格的魁蚶潜沙率差异性分析[J]. 广西科学院学报, 2017, 33(2): 102-107. LIU E F, LIU G B, QIU Z X, et al. The analysis of burrowing rate with different sizes and different bottom sowing time of Scapharca broughtonii[J]. Journal of Guangxi Academy of Sciences, 2017, 33(2): 102-107. |
| [7] |
王扬才, 叶显峰. 饵料藻类对贝类育苗的影响[J]. 齐鲁渔业, 2003, 20(11): 6-8, 12. WANG Y C, YE X F. Effects of feeding algae on molluscan shellfish breeding[J]. Shandong Fisheries, 2003, 20(11): 6-8, 12. |
| [8] |
郑永允, 张晓燕, 栾红兵, 等. 魁蚶生产性控温育苗研究[J]. 齐鲁渔业, 1993(2): 11-14. ZHENG Y Y, ZHANG X Y, LUAN H B, et al. Studies on seed-rearing of Arca inflata by temperature control[J]. Shandong Fisheries, 1993(2): 11-14. |
| [9] |
顾成柏, 焦自芸. 魁蚶控温人工苗种培育技术探索与研究[J]. 齐鲁渔业, 2010, 27(7): 16-17. GU C B, JIAO Z Y. Research and technology to explore the cultivation of arkshell controlled artificial seed[J]. Shandong Fisheries, 2010, 27(7): 16-17. |
| [10] |
叶兆弘, 钟幼平, 贤锋. 饵料对斑玉螺浮游幼虫存活与生长的影响[J]. 台湾海峡, 2001, 20(S1): 49-51. YE Z H, ZHONG Y P, XIAN F. Effects of diets on growth and survival rate for larvae of Natica tigrina[J]. Journal of Oceanography in Taiwan Strait, 2001, 20(S1): 49-51. |
| [11] |
周琳, 于业绍, 陆平. 青蛤幼虫饵料的研究[J]. 海洋科学, 1999, 23(5): 6-7. ZHOU L, YU Y S, LU P. Study on diet of the larvae clam Cyclina sinensis[J]. Marine Science, 1999, 23(5): 6-7. |
| [12] |
冯永勤, 陈华兴, 王建勋. 饵料种类与密度对方斑东风螺(Babylonia areolata (Lamarck))幼虫生长影响的实验研究[J]. 现代渔业信息, 2006, 21(5): 3-7. FENG Y Q, CHEN H X, WANG J X. An experimental study on effect of feed species and density on growth of Babylonia areolata (Lamarck)[J]. Modern Fisheries Information, 2006, 21(5): 3-7. |
| [13] |
何进金, 韦信敏. 菲律宾蛤仔稚贝食料和食性的研究[J]. 水产学报, 1984, 8(2): 99-106. HE J J, WEI X M. A study on food and feeding habit of the clam spat[J]. Journal of Fisheries of China, 1984, 8(2): 99-106. |
| [14] |
孙虎山, 郝刚锋, 王为纲, 等. 紫彩血蛤幼虫适宜饵料的研究[J]. 海洋科学, 1997(4): 4-6. SUN H S, HAO G F, WANG W G, et al. Study on the optimum food for the larvae of Nuttallia oilvacea[J]. Marine Science, 1997(4): 4-6. |
| [15] |
沈伟良, 尤仲杰, 施祥元. 饵料种类和密度对毛蚶浮游幼虫生长的影响[J]. 河北渔业, 2007(9): 18-20, 23. SHEN W L, YOU Z J, SHI X Y. Effect of different kinds and density of live-prey on growth of free-floating larvae of clam Scapharca subcrenata[J]. Hebei Fisheries, 2007(9): 18-20, 23. |
| [16] |
孙虎山, 王为纲, 王宜艳, 等. 饵料密度对紫彩血蛤幼虫生长发育的影响[J]. 烟台师范学院学报:自然科学版, 1998, 14(2): 114-117. SUN H S, WANG W G, WANG Y Y, et al. Influence of density of food on growth and development of larvae of Nuttallia olivacea[J]. Yantai Teachers College Journal:Natural Science, 1998, 14(2): 114-117. |
| [17] |
邱显寅, 郭学武, 王俊. 魁蚶工厂化育苗技术[J]. 海洋水产研究, 1994(15): 71-78. QIU X Y, GUO X W, WANG J. Large scale hatching of S.broughtonii[J]. Marine Fisheries Research, 1994(15): 71-78. |
| [18] |
葛立军, 杨玉香, 梁维波. 不同饵料对毛蚶幼体发育的影响[J]. 水产科学, 2008, 27(5): 226-229. GE L J, YANG Y X, LIANG W B. The effect of different diets on the growth of larval clam Scapharca subcrenata[J]. Fisheries Science, 2008, 27(5): 226-229. |
| [19] |
张善发, 邓岳文, 王庆恒, 等. 几种饵料对华贵栉孔扇贝浮游幼虫生长和成活率的影响[J]. 水产科学, 2008, 27(4): 184-186. ZHANG S F, DENG Y W, WANG Q H, et al. Larval growth and survival in Huagui scallop Chlamys nobilis fed different diets[J]. Fisheries Science, 2008, 27(4): 184-186. |
| [20] |
何连金, 陈文龙, 许万竹, 等. 泥蚶幼虫及稚贝饵料的研究[J]. 福建水产, 1988(1): 28-33. HE L J, CHEN W L, XU W Z, et al. Study on the larvae and juveniles feed Tegillarca ranosa[J]. Fujian Fisheries, 1988(1): 28-33. |
 2017, Vol. 33
2017, Vol. 33 


