2. 南方锰业集团有限责任公司大新锰矿分公司,广西南宁 532315
2. South Manganese Group limited, Daxin Manganese Mine Branch, Nanning, Guangxi, 532315, China
锰是一种重要的战略资源,广泛应用于钢铁、锰合金及锰电池等多个方面。广西是我国锰矿探明储量第一的产区,其探明储量占全国总储量的38.5%,但大部分为低品位贫锰矿,占比为76.91%,而富矿石仅占3.75%[1]。此外,经过长期开采,高品位锰矿资源锐减,综合利用低品位锰矿资源对于缓解我国锰矿资源紧张及提高企业效益具有实际意义。近年来,随着浸提环保要求的提高,生物有机物浸提[2],如蔗渣[3]、糖蜜酒精废液[4-6]也运用在低品位的矿物浸提上,为人们提供以废治废、资源化利用的新途径。但由于有机废液组成复杂,与矿物进行混合后,各有机组分反应活化不同,尾水并未能达到排放标准。此外,有机废液与矿物混合,一方面加大了后期对金属净化分离的难度,另一方面,废液中增加的金属、矿浆及其他成分进一步增加了后期废液的生化处理难度。
微生物燃料电池(Microbial Fuel Cell, MFC)是近年迅速发展起来的一种废水处理技术,也是一种利用微生物的催化作用,将有机物中的化学能转化为电能的电化学装置。微生物燃料电池利用底物广泛,产电过程中几乎没有其他形式的能量耗散,具有较高的理论能量转化效率。目前,以希瓦菌属(Shewanella)和地杆菌属(Geobacter)为模式菌株,通过对Shewanella中的Quinones、CymA与MtrCAB途径,Geobacter中的OMCs系统及pili纳米导线的研究,人们对细胞色素、pili纳米导线、内生电子介质的胞外电子传递过程有了一定的认识[7]。此外,在MFC基础上衍生出来的微生物电解池(Microbial Electrolysis Cell, MEC)[8, 9]与微生物脱盐燃料电池(Microbial Desalination Cell, MDC)[10-12],可用于生物制氢、脱盐或海水淡化,进一步扩大MFC在多领域中的运用。特别是近几年微生物电合成(Microbial Electrosynthesis,MES)的出现,由于能利用电能作为能量输入,驱动还原CO2或有机物合成,将电能转化为化学能,成为人们关注的焦点[13]。
近几年MFC也见于重金属废水处理[14]、土壤修复研究与矿物的湿法浸提应用研究中[18]。该技术主要利用高价态重金属离子阴极端富集并发还原反应,使其价态稳定或毒性降低。MFC反应中还原氧化分开进行的工作特征,提示可以利用该特征将有机废水的氧化与低品位锰矿浸提还原反应分开进行,从而减少两者混合导致的再次污染问题。但目前,无论是用于土壤修复、原位场地修复还是矿物浸提的MFC反应器,都是在比较温和的反应条件下进行。而为了提高矿物浸提效率,MFC在阴极端会使用到强酸碱或高温反应条件,如何将阳极端微生物反应条件与阴极端极端反应耦合是一大挑战。本研究中,笔者通过改进MFC反应器,探索性地将模拟废水的氧化与低品位锰矿浸提还原反应分开进行,用于矿物的浸提,拟实现废水的资源化利用。
1 材料与方法 1.1 MFC与矿物浸提MFC构造本实验中对照组与矿物浸提MFC反应器均以玻璃材质的H型反应器为原型,每组实验设置2组平行,两极反应器有效容积均为160 mL。对照组的H型反应器主要由阳极室、阴极室及质子交换膜(Nafion117)组成。阳极端采用碳毡作为电极,圆柱形,尺寸为5.5 cm(高)×1.5 cm(直径);阴极端采用石墨棒作为电极,圆柱形,尺寸为5.5 cm(高)×2.5 cm(直径)。以模拟废水作为阳极液,主要成分如下:NH4Cl 0.31 g/L, KCl 0.13 g/L, NaH2PO4·2H2O 3.32 g/L, Na2HPO4·12H2O 10.32 g/L,乙酸钠6.8 g/L,维生素和矿物元素。阴极液用50 mmol/L的K3[Fe(CN)6]磷酸缓冲液(Na2HPO4·12H2O 17.91 g/L,KH2PO4 6.8 g/L)。
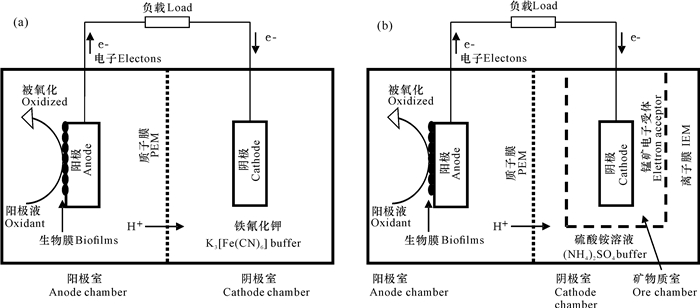
矿物浸提MFC在以上H型反应器基础上改造而成,其阳极室与对照组相同,阴极室在原结构上嵌入一矿物质室组成(图 1),矿物质室通过阳离子交换膜在底部进行物质的隔离与离子的交换。阴电极由石墨电极构成,其尺寸为4 cm(高)×1.5 cm(直径),将其插入被矿物粉末填充的矿物质室内,并通过外线路与石墨阳电极相连接,构成一个完整的电池组。具体制备方法如下:将锰矿粉碎研磨,取过200目筛的软锰矿粉末(MnO2含量为23%) 20 g,先加入少量矿物粉在矿物质室中,加载石墨电极后,再注入剩余矿物粉,边加载边振荡使矿物粉末与石墨电极充分接触压实;然后取10 mL浓度为5%的H2SO4,将三价铁盐Fe2(SO4)3 0.5 g溶于其中,均匀注入矿物质室中,使其成为浆状,混合后用Parafilm封口膜封闭矿物质室开口端,防止溶液蒸发。矿物质室置于1 mol/L的(NH4)2SO4(pH值为5)电解质中。工作过程中,MFC通过外接1 000 Ω电阻形成闭合回路,其输出电压由泓格PISO-813采集卡采集,每隔1 min采集1次电压数据。实验在30℃恒温箱中进行。
|
| 图 1 常规H型MFC反应器与矿物浸提MFC构造图 Fig. 1 MFC structure diagram of conventional H type MFC reactor and mineral extraction |
1.2 矿物成分及反应底物分析
采用高氯酸氧化硫酸亚铁铵滴定法测定矿物中的MnO2含量,处理前后的矿物样品用扫描电镜观察其表面形态,EDS(X射线能量色散谱分析法)对矿物表面微观区域的元素进行分析。XRD(X射线衍射仪)用于矿物成分分析。MFC阳极液中底物的降解程度用化学需氧量(COD)来评估,采用快速消解分光光度法(WTW试剂)测定。
1.3 微生物群落多样性分析对MFC阳极端取0.1 g阳极碳毡,使用PowerSoilTM(MIOBIO)试剂盒提取附着在碳毡上的菌群基因组DNA,DNA样品送至北京诺禾致源科技股份有限公司对16S rRNA的V3区域进行二代高通量测序。
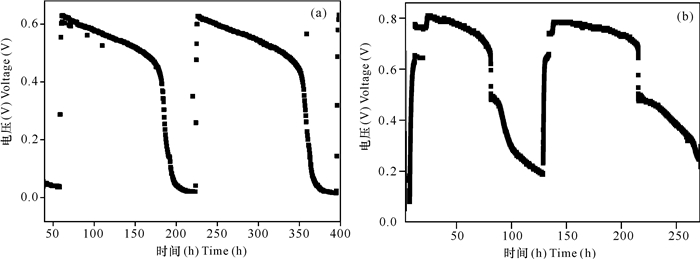
2 结果与分析 2.1 MFC运行过程在运行矿物浸提MFC之前,与对照组进行相同的驯化过程,均以污水厂厌氧污泥作为驯化菌群进行接种。阳极液在接种前及换液过程中均作氮气吹脱处理,阴极液与阳极液同时更换。通过驯化使其菌群在碳毡上着床,产电性能稳定在0.6 V左右,启动矿物浸提MFC。实验持续至阴极端锰矿粉末由黑色变为淡黄色,整个运行时间约为214 d,取同组多个周期进行COD去除率的检测与数据分析,对照组MFC的阴阳两极液及矿物浸提MFC的阳极液均以7 d为一个周期进行更换,而矿物浸提MFC矿物质室的维护以15 d为一个周期,每次补充2 mL 5%的H2SO4溶液维持阴极室的运行。当对照组MFC反应稳定后[图 2(a)],在新的工作周期开始后,短时间内可达到最高电压0.631 V,随着反应的进行,其电压逐渐下降,在117.7 h后,电压降到0.466 V,随后陡然下降,电压稳定139 h后,降到50 mV以下。在矿物浸提MFC反应器中[图 2(b)],其输出电压先在短时间内达到0.74 V,然后在2 h达到最高电压0.781 V,随后逐渐下降,在52.7 h后陡然下降到0.5 V左右,随后电压继续下降最终稳定在0.2 V。当取下降到峰值电压一半作为处理结束点时,在相同碳源条件下,矿物浸提MFC的反应周期为3 d,显著小于对照组MFC 5.19 d的处理时间。通过对两种反应器中阳极液COD的测定,当输出电压降到峰值一半时,对照组COD降到440,相对于起始反应液的COD值3 521,其COD去除率为87.5%;而在矿物浸提MFC中,当电压下降到峰值一半(0.4 V)时,其COD降至320,其去除率为90.9%。矿物浸提MFC的高输出功率增强了对COD的去除能力。
|
| 图 2 矿物浸提MFC与对照组MFC的输出电压曲线 Fig. 2 Voltage output curves of MFC with mineral extraction and control group |
2.2 MnO2的浸提
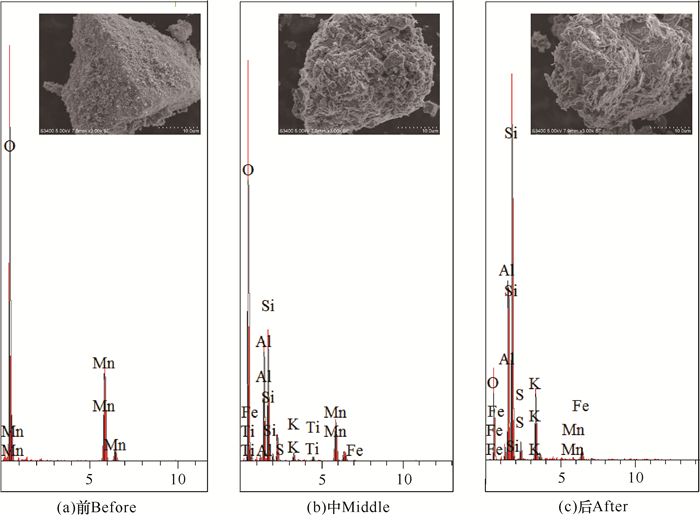
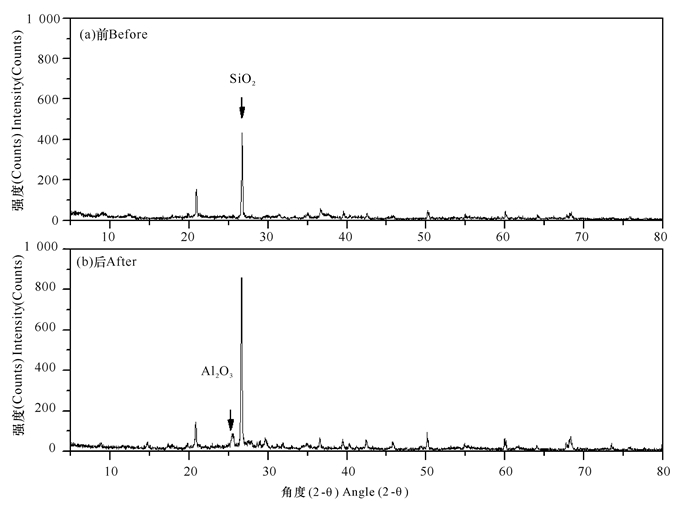
在矿物浸提MFC中,由于阴极室增加了缓冲层,将矿物浸提室与阳极室进行隔离。在矿物浸提室内,矿物粉与酸进行混合浸润后,可接受来自于阳极的电子进行还原反应。当可溶性锰离子或其他可溶性金属离子进入缓冲层后,可以通过缓冲层的(NH4)2SO4对其他的金属除杂,从而实现对锰离子的分离净化,可用于下游的电解硫酸锰。使用EDS分析浸提前后的矿物成分(图 3),其MnO2由浸提前的23%下降到浸提后的0.98%。由于Mn元素的去除,K、Al、Fe、Si元素的含量由原来的1.6%、12.0%、5.12%、13.5%增加到12.7%、18.4%、8.4%、41.7%。XRD的结果也观察到,在处理后SiO2、Al2O3组分样品总含量增加(图 4)。
|
| 图 3 MnO2及矿物浸提前、中、后期矿物成分的电镜与EDS谱图分析 Fig. 3 Analysis of SEM and EDS spectra of MnO2 and minerals before, middle and after leaching |
|
| 图 4 二氧化锰及矿物浸提前后XDR谱图分析 Fig. 4 XDR spectrum analysis of MnO2 and minerals before and after leaching |
2.3 产电微生物的菌群结构分析
为进一步研究矿物浸提MFC反应条件下阳极端菌群结构,利用16S rRNA高通量测序的方法,比较对照组与矿物浸提MFC菌群的种类。在对照组MFC中,Geobacter占总菌群的85%,其后依次是Microvirgula(4.5%),Petrimonas(2.7%),Desulfovibrio(1.8%)。而在矿物浸提MFC中,Geobacter的比例增加,占总菌群的95%,其次分别为Petrimonas(1.1%),Desulfovibrio(0.9%),Microvirgula(0.9%)。结果显示,以乙酸钠为碳源的模拟废水中,尽管Geobacter为严格的厌氧菌,但在半开放操作的MFC中依然占据微生物菌群的主要地位。在以乙酸钠为碳源的MFC反应器中,Geobacter在阳极端是较为常见且占主要地位的菌群类型,本实验对照组MFC中也观察到类似的结论。在矿物浸提MFC反应器中,Geobacter的比例为95%,高于对照组(85%),与MFC产电性能呈正相关关系。该结果提示在以乙酸钠为碳源的反应液中,高的产电性能有利于Geobacter微生物的富集。
3 讨论由于广西地处亚热带,光照时间长,有着丰富的生物资源,微生物[19]、农业废弃物蔗渣[3]、糖蜜酒精废液[4]等也常用于低品位锰矿湿法浸提的研究,这为人们提供了以废治废、资源化利用的新途径。其中,最为常见的是使用甘蔗糖蜜酒精废水,主要原因为广西是全国糖业主产区(占全国产量的66%以上),其副产物糖蜜用于发酵生产酒精,会产生大量甘蔗糖蜜酒精废水,占广西工业有机废水排放的70%。但由于有机废液组成复杂,含有还原性羟基、醛基以及类似的其他复杂基团,包括还原单糖、多糖、纤维素、半纤维素等多种组分,与矿物混合后,各有机组分反应活化不同,虽然浸提后最终反应液中COD、BOD或色素能部分去除,但并未达到排放标准。这种有机废液与矿物的混合物,一方面增加对锰元素纯化的难度,另一方面废液中增加的金属、矿浆及其他成分,加大了浸提液的处理难度。通过本实验的开展,矿物浸提MFC给复杂性有机废水用于低品位锰矿的浸提提供了新的思路,即通过MFC的反应特征将MnO2还原与有机物的氧化分开进行,从而避免直接混合反应中有机废液尾端处理及锰元素的净化问题。
尽管MnO2作为锰电池的放电机制已有大量报道,如Mn4+在酸性条件下,会从阴极端接收电子生成可溶性锰离子Mn2+ (MnO2+4H++2e→Mn2++2H2O),但由于锰矿是多元属组成的复杂体系,除二氧化硅、二价四价锰外,锰矿还附合铁、铝、铅、锌、镁、银等金属元素。在复杂体系中许多金属离子在溶液中都不是以简单离子形态存在,如常规硫铁矿对锰矿的湿法浸提工艺中[20],MnO2在稀硫酸溶液中主要是通过硫铁矿产生的亚铁离子还原与溶解,主要反应为
2MnO2+2Fe2++8H+→2Mn2++2Fe3++4H2O,
FeS2+14Fe3++8H2O→15Fe2++16H++2SO42-。
其中,MnO2被Fe2+还原为Mn2+,而硫铁矿被氧化为Fe3+,这两个氧化-还原反应循环进行,可不断还原浸出低品位锰。此外,在FeSO4对锰矿的浸提过程中,在不同酸度中铁离子还会以不同的物相存在溶液中[21]。如在弱碱性条件下,铁会以Fe(OH)3形式析出溶液,而在酸性条件下主要以Fe3+离子形式存在浸提溶液中。
MnO2+2FeSO4+2H2O→MnSO4+Fe(OH)SO4+Fe(OH)3,
MnO2+2FeSO4+H2SO4→MnSO4+2Fe(OH)SO4,
MnO2+2FeSO4+2H2SO4→MnSO4+Fe2(SO4)3 +2H2O。
在实验过程中,笔者观察到锰矿物浆中酸度与Fe2+/Fe3+两个因素对MnO2浸出速率与输出电压值影响较大。结合以上结论,在矿物浸提MFC阴极端其总体反应应为Fe3+在阴极上还原生成低态Fe2+后,继而与MnO2发生氧化还原反应(MnO2+2Fe2++4H+→Mn2++2Fe3++2H2O),而Fe2+/Fe3+在矿物浸提过程得到循环利用。因此,通过增加外源Fe2+/Fe3+离子可增加矿物浸提MFC的输出电压。
4 结论本实验构建的矿物浸提MFC反应器可以较好地耦合阳极端产电微生物温和的反应条件与阴极极端的反应条件,为MFC用于有机废水处理及低品位锰矿浸提资源化提供了新途径。通过浸提机理的探讨,酸性条件Fe2+/Fe3+循环利用可能是MnO2浸提价态下降的主要方式。矿物浸提MFC进一步发展,可以延伸到重金属废水处理、土壤/场地修复、氧化型矿物浸提等应用场景中,从而扩展MFC现实应用领域。
| [1] |
范娜, 田凤鸣. 广西锰矿资源的可供性分析[J]. 中国矿业, 2009, 18(6): 90-95. DOI:10.3969/j.issn.1004-4051.2009.06.026 |
| [2] |
黄秀兰, 李毅恒, 冯康露, 等. 生物有机物还原软锰矿研究进展[J]. 中国锰业, 2017, 35(6): 140-145. |
| [3] |
崔益顺. 蔗渣还原硫酸浸取低品位软锰矿工艺研究[J]. 无机盐工业, 2013, 45(10): 45-47. DOI:10.3969/j.issn.1006-4990.2013.10.015 |
| [4] |
吕奕菊, 谭家栩, 蒋世权, 等. 糖蜜酒精废液多组分有机物耦合浸出软锰矿动力学研究[J]. 湿法冶金, 2018, 37(1): 20-27. |
| [5] |
高玉洋, 粟海锋, 文衍宣. 半氧化锰矿的直接还原浸出工艺研究[J]. 广西大学学报(自然科学版), 2013, 38(3): 632-637. DOI:10.3969/j.issn.1001-7445.2013.03.021 |
| [6] |
粟海锋, 吕奕菊, 崔勃焱, 等. 糖蜜酒精废液中大分子焦糖色素模拟物浸出软锰矿的动力学[J]. 高校化学工程学报, 2011, 25(1): 43-48. DOI:10.3969/j.issn.1003-9015.2011.01.008 |
| [7] |
布鲁斯·洛根. 微生物燃料电池[M]. 北京: 化学工业出版社, 2009.
|
| [8] |
CALL D, LOGAN B E. Hydrogen production in a single chamber microbial electrolysis cell lacking a membrane[J]. Environmental Science & Technology, 2008, 42(9): 3401-3406. |
| [9] |
LOGAN B E, CALL D, CHENG S, et al. Microbial electrolysis cells for high yield hydrogen gas production from organic matter[J]. Environmental Science & Technology, 2008, 42(23): 8630-8640. |
| [10] |
BETTS K. Using microbes and wastewater to desalinate water[J]. Environmental Science & Technology, 2009, 43(18): 6895. DOI:10.1021/es902384g |
| [11] |
CHEN S S, LIU G L, ZHANG R D, et al. Development of the microbial electrolysis desalination and chemical-production cell for desalination as well as acid and alkali productions[J]. Environmental Science & Technology, 2012, 46(4): 2467-2472. |
| [12] |
SAEED H M, HUSSEINI G A, YOUSEF S, et al. Microbial desalination cell technology: A review and a case study[J]. Desalination, 2015, 359: 1-13. DOI:10.1016/j.desal.2014.12.024 |
| [13] |
朱华伟, 张延平, 李寅. 微生物电合成-电能驱动的CO2固定[J]. 中国科学: 生命科学, 2016, 46(12): 1388-1399. |
| [14] |
MATHURIYA A S, YAKHMI J V. Microbial fuel cells to recover heavy metals[J]. Environmental Chemistry Letters, 2014, 12(4): 483-494. DOI:10.1007/s10311-014-0474-2 |
| [15] |
GUSTAVE W, YUAN Z F, LIU F Y, et al. Mechanisms and challenges of microbial fuel cells for soil heavy metal(loid)s remediation[J]. Science of the Total Environment, 2021, 756: 143865. DOI:10.1016/j.scitotenv.2020.143865 |
| [16] |
ABBAS S Z, RAFATULLAH M. Recent advances in soil microbial fuel cells for soil contaminants remediation[J]. Chemosphere, 2021, 272: 129691. DOI:10.1016/j.chemosphere.2021.129691 |
| [17] |
WU Q, JIAO S, MA M, et al. Microbial fuel cell system: A promising technology for pollutant removal and environmental remediation[J]. Environmental Science and Pollution Research International, 2020, 27(7): 6749-6764. DOI:10.1007/s11356-020-07745-0 |
| [18] |
HUANG T, WEI X, ZHANG S. Bioleaching of copper sulfide minerals assisted by microbial fuel cells[J]. Bioresource Technology, 2019, 288: 121561. DOI:10.1016/j.biortech.2019.121561 |
| [19] |
马皛梅, 韩一凡, 路福平, 等. 功能菌群耦合黄铁矿浸出软锰矿的研究[J]. 微生物学通报, 2012, 39(11): 1551-1559. |
| [20] |
NAYAK B B, MISHRA K G, PARAMGURU R K. Kinetics and mechanism of MnO2 dissolution in H2SO4 in the presence of pyrite[J]. Journal of Applied Electrochemistry, 1999, 29(2): 191-200. DOI:10.1023/A:1003490810114 |
| [21] |
朱道荣. 软锰矿-硫酸亚铁的酸性浸出[J]. 中国锰业, 1992, 10(1): 30-31, 29. |



