2. 广西中药质量标准研究重点实验室, 广西南宁 530022
2. Guangxi Key Laboratory of Tradtitonal Chinese Medicaine Quality Stardands, Nanning, Guangxi, 530022, China
免疫系统最重要的核转录因子(NF-κB)广泛存在于多细胞有机体中,主要通过调控下游靶基因转录参与免疫炎症反应、细胞周期调控、细胞凋亡及细胞黏附等过程。NF-κB信号通路的异常激活通常会介导多种慢性炎症的发生[1, 2],而通路相关蛋白的突变则会导致遗传性疾病的出现或免疫病变,因此开展NF-κB信号通路的研究,在临床炎症的治疗中具有深刻的应用前景。
岗松富含槲皮素、杨梅素等黄酮组分[3-7]。岗松总黄酮(GSH)为本课题组开发的专利产品[8],对体外培养的宫颈癌SiHa细胞增殖、迁移、侵袭具有明显的抑制作用,并促进其凋亡[9],且能显著抑制LPS诱导RAW264.7细胞中TNF-α及IL-6含量,下调iNOS、COX-2蛋白表达[10]。本研究将继续深入考察GSH对炎症因子IL-1β、IL-8、TGF-β,以及NF-κB信号通路中IκBα、NF-κB p65表达的影响,探讨GSH抗炎活性可能的作用靶点。
1 材料与方法 1.1 材料 1.1.1 细胞及培养小鼠RAW264.7单核巨噬细胞(购自中国科学院细胞库),接种于含10%胎牛血清、100 U·mL-1青/链霉素的dMEM培养基中,然后置于5% CO2、37℃培养箱中培养。
1.1.2 药品与试剂岗松药材采收于广西北海市,经广西中医药研究院姜平川研究员鉴定为岗松(Baeckea frutescens L.)的干燥茎叶。MTT(SIGMA),IL-1β、IL-8、TGF-β ELISA试剂盒(RB公司),TRIZOL、TAQ、RNASE INHIB.、dNTP试剂(Life公司), β-actin抗体(江苏康为世纪生物科技股份有限公司), RIPA细胞裂解液(Thermo公司), PBS、蛋白酶抑制剂(Solarbio公司), 预染蛋白marker(Formentas公司);IκBα抗体(CST公司), 碱性磷酸酶标记的马抗小鼠IgG(北京中杉金桥生物技术有限公司), 碱性磷酸酶显色试剂盒(上海碧云天生物技术有限公司), 超纯水;其他试剂为分析纯。
1.1.3 仪器酶标仪(Thermo公司), QPCR(ROCHE公司), 离心机(Eppendorf公司), Fastprep破碎仪(Mpbio公司), 电泳仪(BIO-RAD公司), 半干转膜仪(BIO-RAD公司)。
1.2 方法 1.2.1 GSH的制备[11, 12]将岗松茎叶用70%乙醇(固液比1∶16)进行3次提取,每次提取时间为60 min,过滤合并滤液并浓缩,使岗松提取药液的生药含量为0.3 g·mL-1。用AB-8型大孔吸附树脂填装柱子,将岗松提取药液上柱(1 BV·h-1流速、3 BV体积),用50%乙醇洗脱(2 BV·h-1流速、5 BV用量),浓缩,干燥,即得岗松总黄酮(GSH)。将GSH用DMSO溶解,配制成50, 100, 200 μg·mL-1溶液,备用于细胞试验。
1.2.2 细胞分组及处理取对数生长期的RAW264.7细胞,经0.25 g·L-1胰蛋白酶EDTA消化细胞后,调节细胞浓度至1×106个·mL-1,并接种于细胞培养瓶中。设置实验组分别为空白对照组(以无血清DMEM孵育);LPS模型组(加入0.1 μg·mL-1 LPS孵育24 h);GSH组(设置GSH含量为50, 100, 200 μg·mL-1 3个剂量组,即GSH50、GSH100、GSH200),先GSH预处理细胞2 h后,再加入0.1 μg·mL-1 LPS孵育24 h,待测。
1.2.3 MTT法检测细胞增殖活性分组处理后的细胞,首先置于5% CO2、37℃培养箱中继续培养24 h,弃上清液;接着向每孔加入终质量浓度为1 mg·mL-1的MTT溶液100 μL,并将96孔板移至培养箱中继续孵育4 h后终止培养,吸弃上清液;然后,每孔加入200 μL DMSO溶液,置摇床上50 r/min震荡10 min;最后,于酶标仪上490 nm波长处测定各孔的吸光度。
1.2.4 ELISA法测定细胞中IL-1β、IL-8、TGF-β含量取预处理后的细胞上清液,参照ELISA试剂盒说明书的要求操作,测定IL-1β、IL-8、TGF-β的含量。
1.2.5 WB法检测细胞中IκBα蛋白的相对表达量分组处理后的细胞用冰PBS洗涤,加入蛋白酶抑制剂和磷酸酶抑制剂并收集细胞,经超声破碎后离心处理15 min (12 000 r·min-1,4℃),取上清液待用。采用电泳分离,每孔加25 μg上清液进行上样,分离后的蛋白转移到聚偏氟乙烯膜上,脱脂牛奶封闭,分别用一抗(IκBα、β-actin)孵育过夜,洗膜后,接着用二抗孵育,再次洗膜,显影。通过密度分析测定蛋白含量,目的蛋白的相对含量=目的蛋白密度/β-actin的密度。
1.2.6 QPCR检测细胞中NF-κB p65的mRNA基因表达分组处理后的细胞采用Trizol一步法抽提总RNA,经反转录合成cDNA,其中,总RNA 5 μL、50 μmol·L-1 Oligo(dT) 0.5 μL、10 μmol dNTP 1 μL、DEPC水1 μL。β-actin引物序列:正向引物5′-CATTGTCACCAACTGGGACGATA-3′,反向引物5′-GGATGGCTACGTACATGGCTG-3′;NF-κB p65引物序列:正向引物5′-CACCAAGGATCCACCTCACC-3′,反向引物5′-AATGGCTTGCTCCAGGTCTC-3′。PCR扩增体系为20 μL,反应条件为95℃ 30 s,40个扩增循环(95℃ 10 s,60℃ 30 s,70℃ 45 s),循环完成后测定NF-κB p65的mRNA表达水平。采用相对定量研究分析法,以2-△△Ct比较各组之间NF-κB p65 mRNA表达的差异。
1.2.7 统计学方法实验数据用x±s表示,统计学处理采用单因素方差检验法。
2 结果与分析 2.1 细胞增殖活性的检测由表 1可见,LPS组细胞存活率显著低于空白对照组,表明LPS对RAW264.7细胞具有抑制作用。不同浓度的GSH对LPS诱导的RAW264.7细胞具有显著的保护作用,细胞存活率均有提高。
| 组别 Group |
剂量 Dosage (μg·mL-1) |
细胞存活率 Cell survival rate (%) |
| 空白对照 Blank control |
- | 100.0±2.14** |
| LPS | 0.1 | 63.28±5.07 |
| GSH | 50 | 83.68±4.13* |
| 100 | 95.07±3.81* | |
| 200 | 89.38±6.56* | |
| 注:与LPS组比较,*表示P < 0.05,**表示P < 0.01 Note: Compared with LPS group, * indicates P < 0.05,** indicates P < 0.01 | ||
2.2 IL-1β、IL-8、TGF-β含量的测定
由表 2可见,正常RAW264.7细胞上清液的IL-1β、IL-8、TGF-β含量较低,给予0.1 μg·mL-1 LPS刺激后,IL-1β、IL-8以及TGF-β含量均显著增加,而用50-200 μg·mL-1岗松总黄酮预处理细胞后,IL-1β、IL-8以及TGF-β均受到明显抑制(P < 0.01)。
| 组别 Group |
剂量 Dosage (μg·mL-1) |
IL-1β (pg·mL-1) | IL-8 (pg·mL-1) | TGF-β (pg·mL-1) |
| 空白对照 Blank control |
- | 82.14±12.61** | 76.59±12.46** | 52.50±9.06** |
| LPS | 0.1 | 102.07±22.14 | 139.37±11.84 | 71.53±10.11 |
| GSH | 50 | 69.54±16.32** | 98.42±15.53** | 39.81±7.43** |
| 100 | 51.16±13.78** | 84.16±14.71** | 27.35±9.72** | |
| 200 | 46.52±11.09** | 79.39±17.83** | 22.67±10.09** | |
| 注:与LPS组比较,**表示P < 0.01 Note: Compared with LPS group,** indicates P < 0.01 | ||||
2.3 IκBα蛋白相对表达的检测
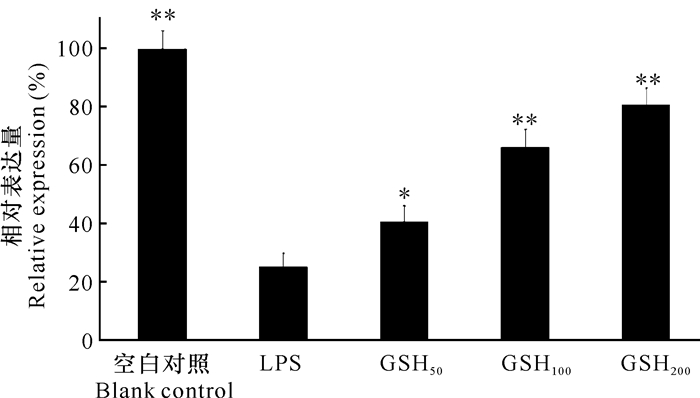
空白RAW264.7细胞IκBα表达较高,给予0.1 μg·mL-1LPS刺激后,IκBα表达明显降低,用不同浓度的GSH预处理细胞后,与LPS组比较,IκBα表达显著回升(P < 0.05或P < 0.01),表明GSH能有效上调炎症细胞中IκBα的表达(图 1和图 2)。

|
| M: 预染蛋白Marker Pre-stained protein marker;1:空白对照组Blank control group;2:LPS组LPS group;3:GSH50; 4:GSH100; 5:GSH200 图 1 GSH对IκBα蛋白表达的影响(x±s,n=6) Fig. 1 Effects of GSH on the expression of IκBα (x±s, n=6) |
|
| 与LPS组比较,*表示P < 0.05,**表示P < 0.01 Compared with LPS group, *indicates P < 0.05, **indicates P < 0.01 图 2 IκBα蛋白相对表达量(x±s,n=6) Fig. 2 Relative expression of IκBα (x±s, n=6) |
2.4 NF-κB p65扩增曲线和溶解曲线
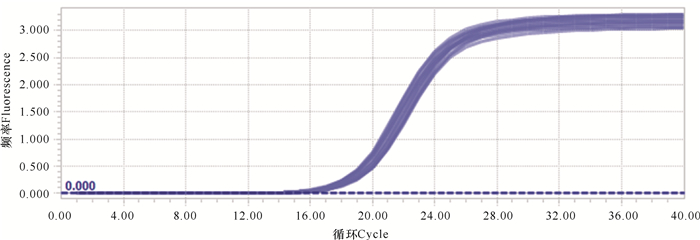
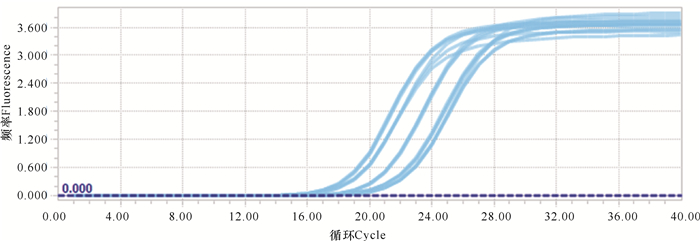
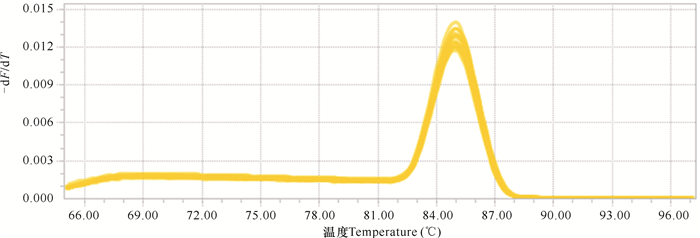
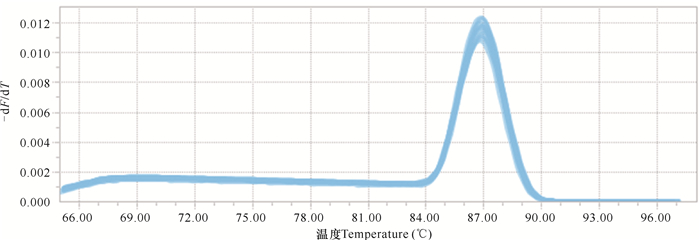
扩增曲线和溶解曲线见图 3-6。从扩增曲线可以看出,荧光强度和初始拷贝数呈良好的线性关系。溶解曲线峰值单一,没有杂峰,表明QPCR产物纯度较高,反应具有良好的特异性。
|
| 图 3 β-actin扩增曲线 Fig. 3 Amplification curve of β-actin |
|
| 图 4 NF-κB p65扩增曲线 Fig. 4 Amplification curve of NF-κB p65 |
|
| 图 5 β-actin溶解曲线 Fig. 5 Solubility curve of β-actin |
|
| 图 6 NF-κB p65溶解曲线 Fig. 6 Solubility curve of NF-κB p65 |
2.5 NF-κB p65的mRNA表达水平的检测
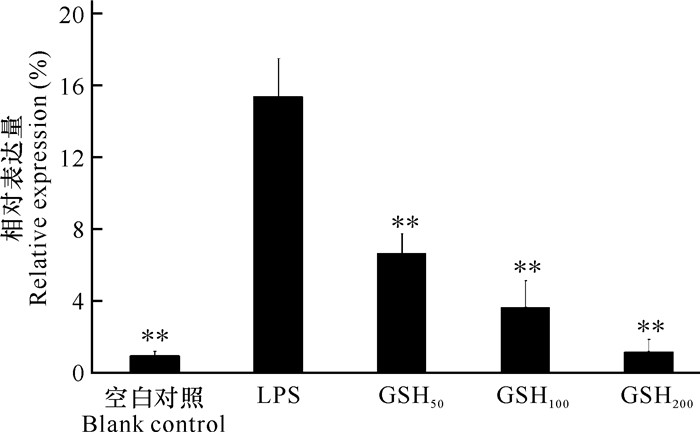
GSH对NF-κB p65 mRNA表达水平的影响结果见表 3及图 7。结果表明,空白RAW264.7细胞NF-κB p65表达较低,给予0.1 μg·mL-1 LPS刺激后,表达明显增强; 用不同浓度的GSH预处理细胞后,与LPS组比较,表达受到明显的抑制(P < 0.01),表明GSH能有效抑制炎症细胞中NF-κB p65的过度表达。
| 组别 Gruop |
剂量 Dosage (μg·mL-1) |
NF-κB p65 | 2-△△Ct |
| 空白对照 Blank control |
- | 20.28±1.83** | 1.00±0.26** |
| LPS | 0.1 | 16.44±2.15 | 15.39±2.10 |
| GSH | 50 | 17.36±2.62** | 6.65±1.12** |
| 100 | 18.29±1.91** | 3.71±1.48** | |
| 200 | 19.90±1.66** | 1.19±0.72** | |
| 注:与LPS组比较,**表示P < 0.01 Note: Compared with LPS group,** indicates P < 0.01 | |||
|
| 与LPS组比较,**表示P < 0.01 Compared with LPS group, **indicates P < 0.01 图 7 NF-κB p65的mRNA相对表达量(x±s,n=6) Fig. 7 Relative expression of NF-κB p65 mRNA (x±s, n=6) |
3 讨论
本课题组通过建立LPS刺激RAW264.7细胞体外模型[13-15],评价GSH对RAW264.7细胞增殖活性的影响,采用ELISA、Western bloting等方法,分析GSH对相关炎症因子(IL-1、IL-6、TGF-β、TNF-α等)和蛋白(iNOS和COX-2等)表达水平的影响。前期实验已证明GSH能显著抑制LPS诱导RAW264.7巨噬细胞中TNF-α及IL-6含量[10],本研究进一步验证:50 μg·mL-1剂量的GSH已经能显著抑制IL-1β、IL-8、TGF-β等炎症因子,并能够显著上调IκBα蛋白表达,表明GSH具有良好的抗炎活性。本实验β-actin和NF-κB p65溶解峰都为单峰,说明本实验的PCR扩增为特异性扩增;同时,定量检测结果显示,GSH能够抑制LPS诱导RAW264.7巨噬细胞中NF-κB p65 mRNA表达。
综上,GSH可促进RAW264.7细胞增殖(P < 0.05),抑制LPS诱导的RAW264.7巨噬细胞中IL-1β、IL-8、TGF-β含量,上调IκBα蛋白表达,抑制NF-κB p65 mRNA表达,表明GSH可能通过抑制NF-κB信号通路,抑制下游炎症因子的表达,从而发挥抗炎活性作用。因此,抑制NF-κB信号通路可能是GSH发挥抗炎活性的一个作用靶点。然而,其具体的作用机制还需要进一步的研究。
| [1] |
COURTOIS G, GILMORE T D. Mutations in the NF-kappa B signaling pathway: Implications for human disease[J]. Oncogene, 2006, 25(51): 6831-6843. DOI:10.1038/sj.onc.1209939 |
| [2] |
NAUGLER W E, KARIN M. NF-kappa B and cancer-identifying targets and mechanisms[J]. Current Opinion in Genetics & Development, 2008, 18(1): 19-26. |
| [3] |
牙启康, 卢文杰, 刘布鸣, 等. 岗松化学成分的研究[J]. 天然产物研究与开发, 2008, 20(5): 827-829, 835. DOI:10.3969/j.issn.1001-6880.2008.05.016 |
| [4] |
卢文杰, 牙启康, 陈家源, 等. 岗松中的一个新黄酮醇苷类化合物[J]. 药学学报, 2008, 43(10): 1032-1035. DOI:10.3321/j.issn:0513-4870.2008.10.009 |
| [5] |
陈家源, 牙启康, 卢文杰, 等. 岗松化学成分的研究[J]. 天然产物研究与开发, 2008, 20(5): 827-829, 835. DOI:10.3969/j.issn.1001-6880.2008.05.016 |
| [6] |
陈明生, 刘布鸣, 林霄, 等. 岗松中杨梅素的含量测定[J]. 时珍国医国药, 2010, 21(11): 2771-2772. DOI:10.3969/j.issn.1008-0805.2010.11.021 |
| [7] |
林霄, 刘布鸣, 陈明生. 高效液相色谱法测定岗松中槲皮素的含量[J]. 时珍国医国药, 2009, 20(1): 102-103. DOI:10.3969/j.issn.1008-0805.2009.01.053 |
| [8] |
刘布鸣, 邱宏聪, 黄艳, 等. 岗松总黄酮的制备及其检测方法: CN201310022966.0[P]. 2013-04-17.
|
| [9] |
马秀珍, 卢艳, 赵冰冰, 等. 岗松总黄酮对宫颈癌SiHa细胞迁移、侵袭及凋亡的影响[J]. 国际肿瘤学杂志, 2021, 48(4): 206-211. DOI:10.3760/cma.j.cn371439-20201119-00041 |
| [10] |
邱宏聪, 张伟, 赵冰冰, 等. 岗松总黄酮体内外抗炎作用研究[J]. 中药材, 2015, 38(8): 1710-1713. |
| [11] |
邱宏聪, 刘布鸣. 星点设计-效应面法优选岗松总黄酮提取工艺[J]. 中国实验方剂学杂志, 2013, 19(12): 46-49. |
| [12] |
邱宏聪, 刘布鸣, 孙翠. 岗松总黄酮的纯化工艺优选[J]. 中国实验方剂学杂志, 2013, 19(13): 34-36. |
| [13] |
刘燕芳, 刘丹, 刘兰, 等. 应用于天然产物抗炎活性研究的主要细胞模型[J]. 天然产物研究与开发, 2020, 32(5): 874-881. |
| [14] |
邵紫君, 李志满, 于鹏程, 等. 氨基酸转化三七花中稀有人参皂苷及提取液对脂多糖诱导的RAW264.7细胞活性的影响[J]. 中草药, 2021, 52(3): 702-710. |
| [15] |
余玲, 康倩, 刘葭, 等. 雷公藤红素与吲哚美辛对脂多糖诱导的RAW264.7细胞的协同抗炎作用研究[J]. 中南药学, 2020, 18(11): 1807-1813. |



