2. 岭南师范学院生命科学与技术学院, 广东湛江 524048
2. School of Life Science and Technology, Lingnan Normal University, Zhanjiang, Guangdong, 524048, China
深海微生物对深海特殊生境(高盐、高压、低温、寡营养等)的适应,造就了其区别于陆生微生物的生物合成途径和酶促反应体系,因而具备产生具有新颖化学结构和独特生物活性代谢产物的能力,是开发天然活性药物先导化合物的资源宝库[1]。据统计,2017年被报道的来自微生物的海洋天然产物占总报道化合物的57%[2]。2018年,张长生等[3]着眼于生态环境、物种多样性和应用领域等方面,指出海洋微生物的研究是一个充满着机遇和挑战的领域。真菌是海洋微生物中重要的类群之一,其代谢产物丰富,且具有新奇的化学结构以及显著的生物活性[4],具有巨大的发展潜力。2017年,高啸巍等[5]对深海真菌Acaromyces ingoldii FS121次级代谢产物进行分离得到化合物22-四烯-3-酮,该化合物在100 μg/mL浓度下,对SF-268、MCF-7、NCI-H460和HepG-2这4种肿瘤细胞株表现出显著的增殖抑制活性, 其半数抑制率IC50值分别为5.3,6.5,12.2和6.1 μmol/L。2018年,马新华等[6]对南海深海沉积物来源真菌Aspergillus sp.MCCC3A400414次级代谢产物的化学成分和生物活性进行研究,从中分离得到5个化合物,即(22E, 24R)-麦角甾-5, 7, 22-三烯-3β-醇、WIN 64821、diorcinol、9-十八碳烯酸和9, 12-十八碳二烯酸。WIN 64821对肿瘤细胞株PANC-1、MCF-7、HepG-2和A549表现出中等强度的细胞毒活性,其IC50值在7.14—15.78 μmol/L[6]。2019年,陈闪冲等[7]从深海真菌Phomopsis tersa的次级代谢产物中分离得到5α,8α-表二氧麦角甾-6, 22-二烯-3β-醇和麦角甾醇,这2个化合物对SF-268、MCF-7、HepG-2和A549 4种肿瘤细胞株具有一定的细胞毒活性。
虽然深海真菌的次级代谢产物结构丰富、活性广泛,但开发程度较低,仍存在较大的挖掘空间。真菌Trichobotrys effuse DFFSCS021分离自我国南海北部2 403 m深的海底沉积物中,纯菌株菌落呈绒状,展开,有凹沟,直径2—3 cm,中央淡粉色周围白色,中间有小气孔。2016年,Sun等[8]从该菌中分离得到3个新的大环内酯类化合物trichobotryside A、trichobotrysides B-C,其中trichobotryside A具有较强的抗生物污损活性,对草苔虫和藤壶幼虫的半数最大效应浓度(EC50)值分别为7.3和2.5 μg/mL。为进一步发掘结构新颖、活性显著的新型化合物,本实验对真菌Trichobotrys effuse DFFSCS021的次级代谢产物进行研究,以期丰富其次级代谢产物的结构类型,为海洋药物先导化合物的开发与利用提供物质基础。
1 材料与方法 1.1 仪器与材料Bruker Avance DRX-500MHz型超导核磁共振仪(内标为TMS:德国布鲁克仪器有限公司)、N-1210B型(EYELA)旋转蒸发仪(上海爱郎仪器有限公司)、LC-20AD型高效液相色谱仪(岛津企业管理(中国)有限公司)、YMC-PACKODS-A型分析色谱柱(规格:150×4.6 mml.D.S - 5 μm,12 nm)、YMC-PACKODS-A型半制备色谱柱(规格:250×10 mml.D.S-5 μm,12 nm),Bruker microTOF-QⅡ高分辨电喷雾质谱仪(HR-ESI-MS)、Bruker amaZonSL低分辨电喷雾质谱仪(ESI-MS)(布鲁克(北京)科技有限公司),iMark酶标仪(美国BIO-RAD公司)、MCO-175型CO2培养箱(日本Sanyo公司)、SW-CJ-2FD型超净工作台(苏州净化设备公司)、ZF-7型三用紫外分析仪(上海顾村电光仪器厂)、CCA-1112A型冷却水循环装置(上海爱郎仪器有限公司)、SB-800DT型超声波清洗器(宁波新芝生物科技股份有限公司)、Direct-Q5UV-R型超纯水一体机(默克密理博(上海)实验设备科技有限公司)、JJ-2型组织匀浆机(常州澳华仪器有限公司),所用试剂均为分析纯。
深海真菌Trichobotrys effuse DFFSCS021,采自南海北部(112°30.203′E, 18°1.654′N) 2 403 m深的海底沉积物中,经分离培养纯化后得到纯菌株保藏于中国科学院海洋微生物中心。
1.2 方法 1.2.1 菌株鉴定深海真菌Trichobotrys effuse DFFSCS021的总DNA按照文献[9]方法提取,设计引物对总DNA中的ITS序列进行PCR扩增,回收纯化扩增产物并连接到PCR21载体(Invitrogen)中。16S rRNA基因序列送生工生物工程(上海)股份有限公司测定,将测得的16S rRNA基因序列进行BLAST分析,发现其与T.effusa isolate 1179 (accession No.KJ630313)相似度为99%。
1.2.2 菌株的发酵培养从PDA固体培养基平板上,用接种环刮取2环该菌株的孢子, 接种于盛有PDA液体培养基的三角锥形瓶中,置于摇床上180 r/min、28℃恒温培养3—7 d,待三角锥形瓶中菌丝体生长成球形黄豆粒大小时,将生长好的种子液接种到含80 g大米培养基的1 L三角瓶中,每瓶接种10 mL,共接种50瓶,28℃静置30 d。
PDA液体培养基:马铃薯200 g,葡萄糖20 g,海盐36 g,蒸馏水溶解定容至1 000 mL。固体培养基在此基础上添加20 g琼脂。
大米培养基:大米80 g,酵母膏0.4 g,葡萄糖0.4 g,海盐3.6 g,蒸馏水溶解定容至120 mL。
1.2.3 高效液相色谱(HPLC)分析及半制备分析条件:流速为1 mL/min,流动相为MeOH/H2O体系,检测波长为210,254,280,360 nm,柱温箱温度为35℃,进样量为5 μL。半制备条件:流速为3 mL/min,流动相为MeOH/H2O体系,检测波长为210,254,280,360 nm,柱温箱温度为35℃,进样量为60 μL。分析时根据化合物的极性来调整MeOH/H2O的比例,以达到半制备的目的。
1.2.4 发酵产物的提取与分离将发酵好的大米培养基用80%丙酮-水浸泡,接着用组织匀浆机破壁,之后超声30 min,用布氏漏斗抽滤,旋转蒸发除去丙酮,将剩下的水相再用乙酸乙酯进行萃取(V乙酸乙酯:V水=2:1),静置分层,取上层乙酸乙酯相进行浓缩称量,共得到浸膏30 g。
将乙酸乙酯萃取的浸膏30 g经硅胶(100—200目)柱层析,以氯仿/甲醇(体积比1:0—0:1)进行梯度洗脱,最后合并为7个流分(Fr 01—Fr 07)。
流分Fr 05 (4 g)经硅胶(200—300目)柱层析,以氯仿/甲醇(体积比20:1—1:1)梯度进行洗脱,得到4个亚流分(Fr 0501—Fr 0504),亚流分Fr 0502 (280 mg)经Sephadex LH-20凝胶柱层析得到4个亚流分(Fr 050201—Fr 050204),亚流分Fr 050204(80 mg)经半制备HPLC进一步纯化得到化合物1 (V甲醇:V水=10:90,tR= 20.5 min,26 mg)。
流分Fr 03 (7.5 g)经硅胶(200—300目)柱层析,以氯仿/丙酮(体积比50:1—0:1)梯度进行洗脱,得到4个亚流分(Fr 0301—Fr 0304),亚流分Fr 0302 (1 g)经Sephadex LH-20凝胶柱层析得到4个亚流分(Fr 030201—Fr 030204),亚流分Fr 030201 (65 mg)经硅胶(200—300目)柱层析,以氯仿/丙酮(体积比20:1)等度进行洗脱,得到化合物2 (13.5 mg)。
流分Fr 04 (0.7 g)经硅胶(200—300目)柱层析,以氯仿/甲醇(体积比20:1—0:1)梯度进行洗脱,得到4个亚流分(Fr 0401—Fr 0404),亚流分Fr 0401 (244.1 mg)经Sephadex LH-20凝胶柱层析得到3个亚流分(Fr 040101—Fr 040103),亚流分Fr 040103 (45.5 mg)经半制备HPLC进一步纯化得到化合物4 (V甲醇:V水=35:75),tR=30.5 min,4.9 mg)。亚流分Fr 0402 (122.6 mg)经半制备HPLC进一步纯化得到化合物3 (V甲醇:V水=33:77,tR=28 min,15 mg)。
流分Fr 02 (0.52 g)经硅胶(200—300目)柱层析,以石油醚/氯仿(体积比50:1—0:1)梯度进行洗脱,得到3个亚流分(Fr 0201—Fr 0203),亚流分Fr 0201 (175.9 mg)经半制备HPLC进一步纯化得到化合物5 (V甲醇:V水=85:15,tR=44 min,3.1 mg)。
1.2.5 细胞毒活性测定参照文献[10]的方法,取对数生长期的肿瘤细胞,将细胞密度调至2×105个/mL,按每孔200 μL加到96孔细胞培养板中,放入37℃培养箱中并通入体积分数5% CO2,培养4 h。化合物样品分别设定5个浓度梯度,每个浓度设3个重复,同时设阳性、阴性对照,每孔肿瘤细胞中分别加样品液或空白液2 μL,再培养72 h。然后每孔加四甲基偶氮唑蓝(MTT)液10 μL,继续培养4 h,在37℃、2 000 r/min条件下,离心8 min,吸去上清液。每孔分别加入二甲基亚砜(DMSO)100 μL,在微量振荡器上振荡15 min,至结晶完全溶解后,用酶标仪测定每孔在570 nm处的吸光值(OD值)。取3孔平均OD值,按对细胞增殖的抑制率(IR,%)=[(OD空白-OD样品)/OD空白]×100%, 计算样品IR,并采用bliss法计算出半数抑制率IC50。
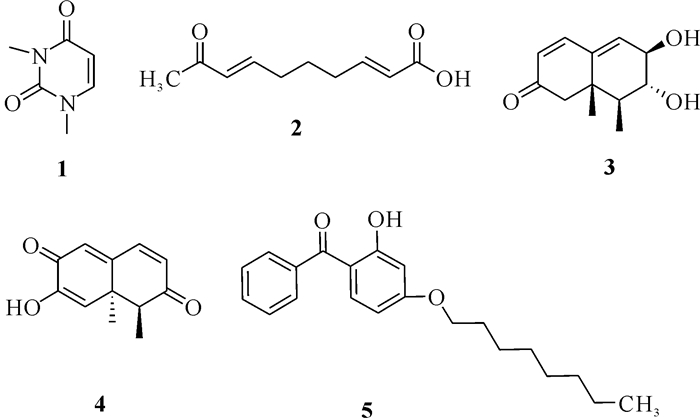
2 结果与分析 2.1 化合物结构鉴定化合物1—5的结构如图 1所示。
|
| 图 1 化合物1—5的结构 Fig. 1 Structures of compounds 1—5 |
化合物1:白色无定形粉末。1H NMR(500 MHz, CDCl3) δH 7.12(1H, d, J= 7.5 Hz, H-6), 5.74(1H, d, J=7.5 Hz, H-5), 3.80(3H, m, 1-NCH3), 3.35(3H, m, 3-NCH3)。13C NMR(125 MHz, CDCl3)δ:162.3(s, C-4), 151.4(s, C-2), 144.6(d, J=5.5 Hz, C-6), 102.4(d, J=5.5 Hz, C-5), 36.7(s, 3H), 28.2(s, 3H)。低分辨质谱(+)-ESIMS给出准分子离子峰m/z 141.1[M+H]+和281.1[2M+H]+,(-)-ESIMS给出准分子离子峰m/z 139.3 [M-H]-。上述氢谱和质谱数据与文献报道的数据[11]一致,故鉴定该化合物为1, 3-dimethyluracil。
化合物2:无色油状物。1H NMR (500 MHz, CDCl3) δH 7.05(1H, dd, J1=7.0 Hz, J2=15.5 Hz, H-3), 6.78(1H, dd, J1=6.5 Hz, J2=16.0 Hz, H-7), 6.09(1H, d, J=16.0 Hz, H-8), 5.85(1H, d, J=15.5 Hz, H-2), 2.29(2H, m, H-4), 2.28(2H, m, H-6), 2.26(3H, s, H-10), 1.67(2H, m, H-5);13C NMR(125 MHz, CDCl3)δC198.5(C, C-9), 170.6(C, C-1), 150.8(CH, C-3), 146.9(CH, C-7), 131.8(CH, C-8), 121.2(CH, C-2), 31.7(CH2, C-4), 31.6(CH2, C-6), 21.7(CH3, C-10), 26.3(CH2, C-5)。(+) -HRESIMS给出的分子式为C10H15O3(m/z 183.101 5 [M+H]+,calcd.for C10H15O3, 183.101 6)。上述数据与文献[12]一致,故鉴定该化合物为[2E, 7E]-9-oxo-2, 7-decadienoic acid。
化合物3:无色粉末。1H NMR (500 MHz, CDCl3) δH 6.88(1H, d, J=10.0 Hz, H-1), 5.80(1H, s, H-9), 5.93(1H, d, J=10.0 Hz, H-2), 4.24 (1H, d, J=7.0 Hz, H-8), 3.87(1H, m, H-7), 2.45(1H, dd, J1=6.5 Hz, J2=13.5 Hz, H-4), 1.97(1H, dd, J1=2.5 Hz, J2=12.5 Hz, H-6a), 1.65(1H, t, J=12.5 Hz, H-6b), 1.07(3H, s, H-12), 1.06(3H, s, H-11);13C NMR (125 MHz, CDCl3)δC200.8(C, C-3), 143.8(CH, C-1), 142.1(C, C-10), 131.8(CH, C-9), 127.2(CH, C-2), 74.4(CH, C-8), 70.0(CH, C-7), 53.2(CH, C-4), 42.0(CH2, C-6), 41.2(C, C-5), 20.1(CH3, C-12), 7.2(CH3, C-11)。(+) -HRESIMS给出的分子式为C12H17O3 (m/z 209.078 7 [M+H]+,calcd.for C12H17O3, 209.078 1)。上述数据与文献[13]报道一致,故鉴定该化合物为periconianones H。
化合物4:无色粉末。1H NMR(500 MHz, CDCl3) δH 7.21(1H, d, J=10.0 Hz, H-9), 6.30(1H, d, J=10.0 Hz, H-8), 6.53(1H, s, H-1), 6.38(1H, s, H-4), 2.53(1H, dd, J1=7.0 Hz, J2=13.5 Hz, H-6), 1.25(3H, s, H-11), 1.31(3H, d, J=7.0 Hz, H-12);13C NMR(125 MHz, CDCl3)δC198.6(C, C-7), 181.1(C, C-2), 160.8(C, C-10), 147.3(C, C-3), 141.6(CH, C-9), 131.8(CH, C-8), 125.9(CH, C-1), 123.1(CH, C-4), 50.9(CH, C-6), 45.2(C, C-5), 23.4(CH3, C-11), 8.2(CH3, C-12)。(+) -HRESIMS给出的分子式为C12H13O3(m/z 205.086 0 [M+H]+,calcd.for C12H13O3, 205.085 9)。上述数据与文献[14]报道一致,故鉴定该化合物为botryosphaeridione。
化合物5:无色油状物。1H NMR(500 MHz, CDCl3) δH 7.48(1H, m, H-6), 7.56(1H, m, H-4′), 7.63(2H, m, H-6′, H-2′), 7.49(2H, m, H-5′, H-3′), 6.40(1H, dd, J1=2.5 Hz, J2=9.0 Hz, H-5), 6.50(1H, d, J=2.5 Hz, H-3), 4.02(2H, m, H-8), 1.30(2H, m, H-13), 1.26(2H, m, H-11), 1.33(2H, m, H-12), 1.80(2H, m, H-9), 1.46(2H, m, H-10), 1.28(2H, m, H-14), 0.89(3H, s, H-15);13C NMR(125 MHz, CDCl3)δC200.1(C, C-7), 166.3(C, C-2), 165.8(C, C-4), 138.3(C, C-1′), 135.2(CH, C-6), 131.4 (CH, C-4′), 128.9(CH, C-6′, C-2′), 128.3(CH, C-5′, C-3′), 113.0(C, C-1), 107.8(CH, C-5), 101.5(CH, C-3), 68.5(CH2, C-8), 31.8(CH2, C-13), 29.3(CH2, C-11), 29.2(CH2, C-12), 28.9(CH2, C-9), 26.0(CH2, C-10), 22.7(CH2, C-14), 11.4(CH3, C-15)。(+) -HRESIMS给出的分子式为C21H27O3 (m/z 327.196 1 [M+H]+,calcd.for C21H27O3, 327.195 5)。上述数据与文献[15]报道一致,故鉴定该化合物为2-hydroxy-(4-octyloxy)benzophenone。
2.2 化合物活性测定化合物3对人肝癌细胞(HepG-2)、人食管癌细胞(Eca109)、人急性骨髓白血病细胞(KG-1a)、人前列腺癌细胞(PC-3)和人喉癌细胞(Hep2)均未显示出细胞毒活性,仅对人宫颈癌细胞(Hela)显示出弱的抑制活性,其IC50值为20.5 μmol/L (表 1)。该结果与文献[13]报道的化合物periconianones H对Hela显示出弱的细胞毒活性(IC50=16.5 μmol/L)的结果较为一致。
| 化合物 Compound |
细胞毒活性IC50Cytotoxic activity IC50 (μmol/L) | |||||
| HepG-2 | Hela | Eca109 | KG-1a | PC-3 | Hep2 | |
| 3 | > 100 | 20.5±2.15 | > 100 | > 100 | > 100 | > 100 |
| Periconianones H[13] | - | 16.5 | - | - | - | - |
| 阿霉素Doxorubicin | 3.34±0.96 | 0.85±0.00 | 0.23±0.00 | 0.72±0.00 | 1.60±0.16 | 0.02±0.00 |
| 注:“—”代表未检出 Note:“—” represents undetectable |
||||||
3 结论
本研究对来源于南海北部2 403 m深的海底沉积物中1株真菌Trichobotrys effuse DFFSCS021的乙酸乙酯萃取物进行化学成分研究,从中获得5个单体化合物,分别为1, 3-dimethyluracil (1)、[2E, 7E]-9-oxo-2, 7-decadienoic acid (2)、periconianones H (3)、botryosphaeridione (4)和2-hydroxy-(4-octyloxy) benzophenone (5),均为首次从该菌株中分离得到。对化合物3进行细胞毒活性筛选,结果表明该化合物对5株肿瘤细胞株HepG-2、Eca109、KG-1a、PC-3和Hep2均未显示出细胞毒活性,仅对Hela显示弱的抑制活性。另外,据报道,化合物4对双子叶植物莴苣的种子萌发具有显著的抑制活性[14],化合物2,5的活性数据未见报道。接下来将对剩余的4个化合物进行多种生物活性筛选,例如抑制种子萌发、抗菌以及抗生物污损等,以期为进一步研究该菌属的海洋真菌提供活性数据和参考资料。
| [1] |
宋双, 许佳怡. 海洋来源的曲霉属真菌次级代谢产物及其活性研究进展[J]. 中山大学研究生学刊:自然科学、医学版, 2015, 36(3): 20-32. |
| [2] |
CARROLL A R, COPP B R, DAVIS R A, et al. Marine natural products[J]. Natural Product Reports, 2019, 36(1): 122-173. |
| [3] |
张长生, 李文利. 海洋微生物学:新机遇, 新挑战[J]. 微生物学通报, 2018, 45(9): 1841-1842. |
| [4] |
曾奇, 仲伟茂, 王发左. 深海来源真菌次级代谢产物研究进展[J]. 天然产物研究与开发, 2018, 30(3): 501-514. |
| [5] |
高啸巍, 陈玉婵, 孙章华, 等. 深海真菌Acaromyces ingoldii FS121次级代谢产物及其细胞毒活性[J]. 中药材, 2017, 40(2): 359-363. |
| [6] |
马新华, 郑卫敏, 周芳, 等. 2株深海来源真菌次级代谢产物的研究[J]. 中国海洋药物, 2018, 37(5): 41-46. |
| [7] |
陈闪冲, 陈玉婵, 李赛妮, 等. 深海真菌Phomopsis tersa的次级代谢产物及其细胞毒活性研究[J]. 中国海洋药物, 2019, 38(6): 8-14. |
| [8] |
SUN Y L, ZHANG X Y, NONG X H, et al. New antifouling macrodiolides from the deep-sea-derived fungus Trichobotrys effuse DFFSCS021[J]. Tetrahedron Letters, 2016, 57(3): 366-370. DOI:10.1016/j.tetlet.2015.12.026 |
| [9] |
LAI X T, CAO L X, TAN H M, et al. Fungal communities from methanehydrate-bearing deep-sea marine sediments in South China Sea[J]. The ISME Journal, 2007, 1(8): 756-762. DOI:10.1038/ismej.2007.51 |
| [10] |
SUN Y L, WANG J, WANG Y F, et al. Cytotoxic and antiviral tetramic acid derivatives from the deep-sea-derived fungus Trichobotrys effuse DFFSCS021[J]. Tetrahedron, 2015, 71(49): 9328-9332. DOI:10.1016/j.tet.2015.10.010 |
| [11] |
KHETRAPAL C L, KUNWAR A C. NMR spectra of oriented biologically important molecules.The structure of and the internal rotation in N, N'-dimethyluracil[J]. Journal of Physical Chemistry, 1982, 86(24): 4815-4817. DOI:10.1021/j100221a032 |
| [12] |
PROKSA B, ADAMCOVÁ J, LIPTAJ T, et al. Identification and determination of organic acids in cultivation medium of Penicillium vermiculatum Dang[J]. Monatshefte Für Chemie-Chemical Monthly, 1994, 125(6/7): 707-711. DOI:10.1007/BF01277630 |
| [13] |
LIU J M, ZHANG D W, ZHANG M, et al. Eremophi-lane sesquiterpenes from an endophytic fungus Periconia species[J]. Journal of Natural Products, 2016, 79(9): 2229-2235. |
| [14] |
ZHANG L, WANG S Q, LI X J, et al. New insight into the stereochemistry of botryosphaeridione from a Phoma endophyte[J]. Journal of Molecular Structure, 2012, 1016: 72-75. |
| [15] |
KHAMIDULLINA E A, PUREVDASH M, USHAKOV I V, et al. Phenolic compounds from Pinus sibirica shells[J]. Chemistry of Natural Compounds, 2005, 41(1): 101-102. DOI:10.1007/s10600-005-0088-9 |



