2. 中国科学院南海海洋研究所, 广东省海洋药物重点实验室, 广东广州 510301
2. Guangdong Key Laboratory of Marine Materia Medica, South China Sea Institute of Oceanology, Chinese Academy of Sciences, Guangzhou, Guangdong, 510301, China
海洋真菌是海洋微生物的重要组成之一,复杂的海洋生态环境使其产生结构多样、活性丰富的次级代谢产物,进而成为天然产物及创新药物的重要来源。海洋真菌约有四分之三分离自海洋生物体,包括植物(藻类、红树和其他高等植物)、海洋无脊椎动物(海绵、珊瑚、海鞘、海参、双壳类、甲壳类)和脊椎动物(主要是鱼类)[1]。海藻共附生真菌主要是指以内生、附生和共生形式存在于藻体组织中的丝状真菌。为适应复杂的海洋生态环境,海藻共附生微生物可产生独特的次级代谢产物参与宿主的防御体系,帮助宿主抵抗外界致病菌和病毒的侵害,以及其他海洋生物的攻击,维护海洋生态系统的平衡。这些具有化学防御功能的微生物次级代谢产物往往结构新颖、生物活性多样,为新型海洋药物的研发提供了宝贵的材料[2]。
自20世纪90年代起,海洋天然产物化学研究者便开始关注海藻共附生真菌,在过去的二十余年,已报道的海藻共附生真菌来源的新天然产物超过400种。这些化合物的结构类型包括聚酮、萜类、肽、生物碱和脂肪酸酯等。据报道,66%的海藻共附生真菌来源的新天然产物具有抗肿瘤、抗菌、抗氧化和杀虫等活性[3, 4],可为海洋药物或生物防治剂的研发提供宝贵的源头分子。本文依据化合物的生物活性进行分类,从抗菌、抗肿瘤、抗氧化、抗炎、浮游生物抑制等方面,对2006年以来海藻共附生真菌来源的新颖活性天然产物研究进行概述,旨在为海藻共附生真菌天然产物研究及其药用研发提供参考依据。
1 海藻共附生真菌来源天然产物分类 1.1 抗菌活性天然产物海藻共附生真菌与宿主相互依存,通过产生活性代谢产物构建化学防御体系,帮助宿主海藻抵抗环境中的致病微生物。因此,抗菌活性是海藻共附生真菌来源的天然产物较为常见的生物活性。
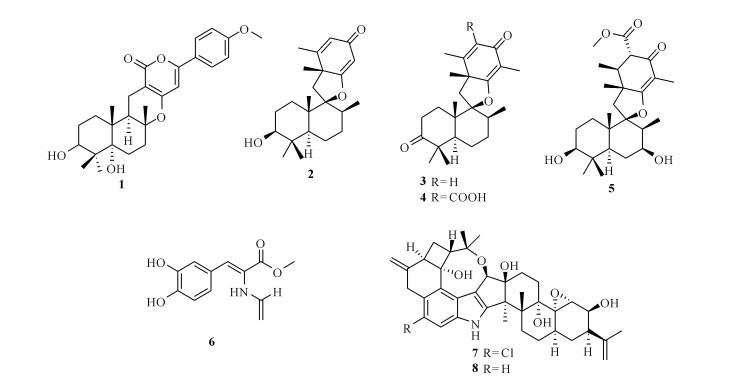
Li等[5]从福建平潭红藻Chondrus ocellatus中分离得到一株青霉菌Penicillium echinulatum pt-4,使用马铃薯葡萄糖琼脂(PDA)培养基静置培养后从其代谢产物中分离得到1个新的混源萜Arisugacin K (1),该化合物对大肠杆菌具有抑制作用(30 μg/disk,抑菌圈直径为8 mm)。
Liu等[6]从红藻Pterocladiella tenuis中分离得到共附生青霉菌Penicillium chermesiltum EN-480,并从其发酵物中分离得到补身烷型倍半萜Chermesins A—D (2—5),其中化合物2和3对大肠杆菌、白色念珠菌、藤黄微球菌和溶藻弧菌都具有一定的抑制活性,最低抑菌浓度为8—64 μg/mL,化合物5对大肠杆菌表现出微弱的抑制作用(MIC为64 μg/mL),而化合物4对所有菌株均无抑菌活性。由构效关系推测该类化合物中C-5′双键或环己二烯酮结构的存在为抑菌活性的关键,而C-5′位羧基基团的存在则明显降低抑菌活性。
Li等[7]从与红藻Codium fragile共生的青霉菌Penicillium oxalicum EN-290代谢物中分离出1个新的酚醛烯胺类化合物(Z)-3-(3, 4-二羟苯基)-2-甲酰胺丙烯酸(6),活性试验结果表明其对金黄色葡萄球菌具有抑制作用,MIC为2.0 μg/mL,抑制作用强于阳性对照氯霉素(MIC为4.0 μg/mL)。
Zhang等[8]从海洋多管藻Polysiphonia scopulorum中分离得到一株真菌Aspergillus nidulans EN-330,使用马铃薯葡萄糖肉汤(PDB)培养基静置发酵30 d后,从其菌丝体丙酮提取物中分离得到1个氯代吲哚二萜19-hydroxypenitrem A (7)和1个无氯衍生物19-hydroxypenitrem E (8),两种化合物对4种病原菌(迟钝爱德华菌、鳗弧菌、大肠杆菌、金黄色葡萄球菌)均具有抑制作用,MIC为16-64 μg/mL。构效关系表明含氯化合物7活性强于无氯化合物8,推测氯原子的引入可提高化合物的活性。
化合物1—8的结构如图 1所示。
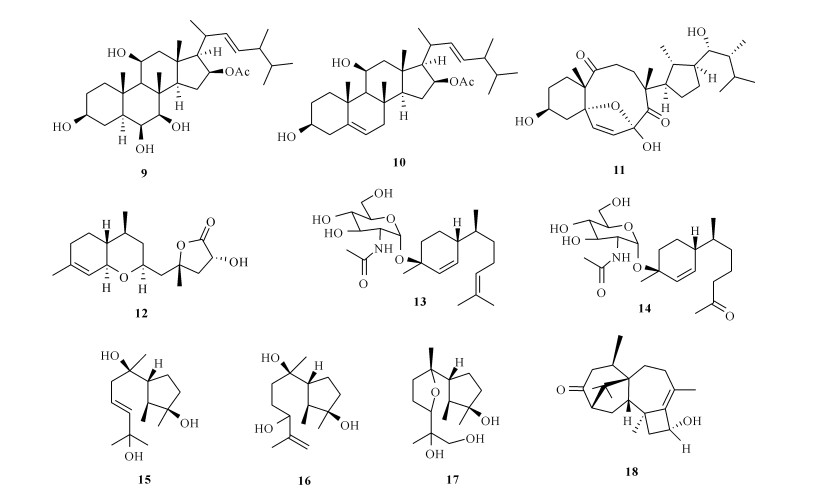
Gao等[9]从海洋红藻中分离出一株青霉属真菌Penicillium chrysogenum QEN-24S,并从其代谢产物中分离得到2个新的类固醇Penicisteroids A和B(9和10);Penicisteroid A (9)对病原性真菌Aspergillus niger和Alternaria brasicae表现出显著的抑制活性,在浓度为20 μg/disk时抑菌圈直径分别为18和8 mm; 化合物9对肿瘤细胞株HeLa、SW1990和NCI-H460具有选择性细胞毒活性,IC50分别为15, 31和40 μg/mL。
Song等[10]从海洋褐藻Sargassum sp.共附生真菌Trichoderma asperellum cf44-2发酵物中分离出一系列骨架新颖的化合物,其中包括结构高度转化的麦角固醇衍生物Tricholumin A (11),活性研究结果表明化合物11具有抗哈维弧菌、灿烂弧菌和假单胞菌的生物活性,当其浓度为50 μg/disk时,抑菌圈直径分别为10,7.5和8.0 mm; 化合物11对植物致病真菌Glomerella cingulata也具有抑制作用,MIC为12 μg/mL。此后,Song等[11]对cf44-2菌株代谢产物进一步挖掘,从中分离出7个新颖的萜类化合物12—18,抗菌活性研究发现:化合物13和14在浓度为20 μg/disk时,对4种弧菌(副溶血性弧菌,鳗弧菌,哈维弧菌和灿烂弧菌)均表现出显著的抑制活性,抑菌圈直径为6.1-6.4 mm,由此推测其抗菌活性的产生可能与2-乙酰氨基-2-脱氧-α-D-吡喃葡萄糖基的存在相关。
以上化合物结构详见图 2。
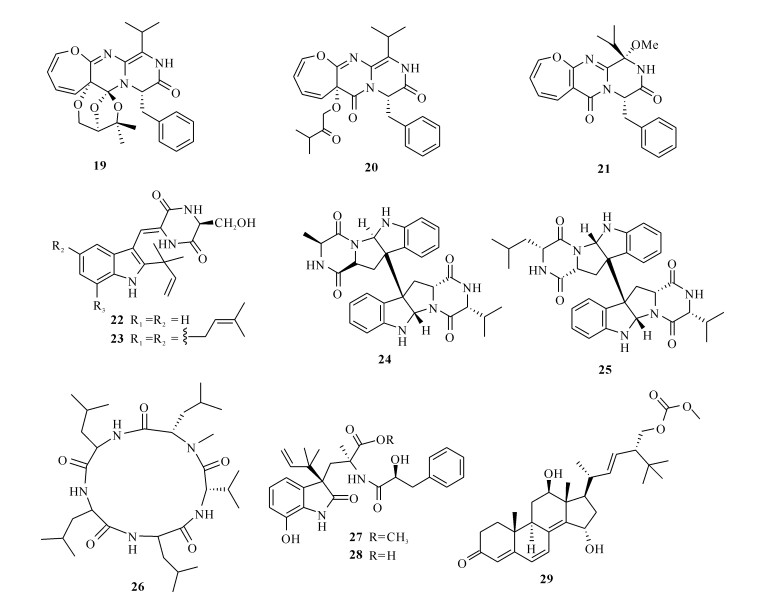
Zhang等[12, 13]从红藻共附生拟青霉属真菌Paecilomyces variotii EN-291次级代谢产物中陆续分离得到3个含二氢二苯恶庚英结构的二酮哌嗪类生物碱Varioxepine A (19)、Varioloids A和B (20和21),活性研究结果表明这些化合物可抑制部分人类致病菌和水生细菌的生长(MIC为16-64 μg/mL),对植物致病真菌禾谷镰刀菌也表现出显著的抑制活性(MIC为4-8 μg/mL)。
Du等[14]从马尾藻Sargassum thunbergii中分离出一株曲霉属真菌Eurotium cristatum EN-220,并从其提取物中分离得到多个活性化合物,其中包括4个新的吲哚类生物碱Cristatumins A-D (22—25)。化合物22对大肠杆菌和金黄色葡萄球菌具有抑制活性,MIC为64 μg/mL;化合物25具有微弱的抗金黄色葡萄球菌的活性,在浓度为100 μg/disk时,抑菌圈直径为8 mm;此外,化合物23对鳃足虫表现出中等杀虫活性,半数致死率LD50为74.4 μg/mL[14]。
Gulder等[15]从美国圣地亚哥拉霍亚海岸采集的一株绿藻中分离得到真菌Asteromyces cruciatus #763,采用单菌多产物(OSMAC)策略筛选发酵后,从其代谢产物中分离得到1个新的五肽化合物Lajollamide A (26),化合物26在100 μmol/L的浓度下对部分革兰氏阳性细菌和致传染性疾病的细菌均表现出较弱的抑制活性,对枯草芽孢杆菌和表皮葡萄球菌的抑制率分别为61%和30%。
Yang等[16]从中国青岛采集的红藻Ceramium japonicum中分离得到一株曲霉属真菌Aspergillus alabamensis EN-547,采用PDA培养基对其进行发酵,并从其乙酸乙酯提取物中分离得到2个新的二酮吗啉衍生物(27和28)和1个新的高共轭麦角甾烷型类固醇(29);化合物27—29对人类病原体(大肠杆菌和藤黄微球菌)和两种水生细菌(爱德华氏菌属和溶藻弧菌)具有抑制作用,MIC为16—64 μg/mL。
化合物19—29的结构详见图 3。
1.2 抗肿瘤活性天然产物
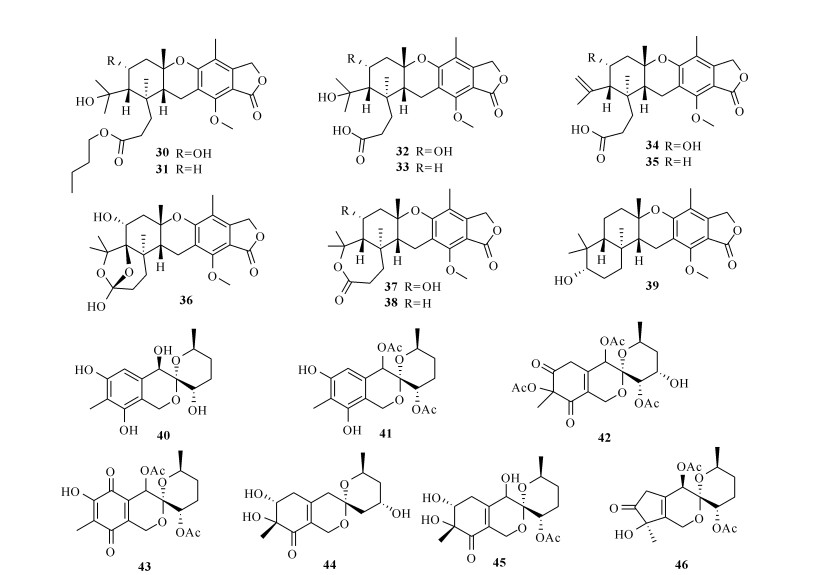
海藻共附生真菌是抗肿瘤活性天然产物的重要生产菌株之一。Zhuravleva等[17]从褐藻共附生青霉菌Penicillium lividum KMM 4663中分离得到混源萜类化合物31—39,从另一株共附生青霉菌Penicillium thomii KMM 4645分离得到混源萜类化合物30-34,37和38。化合物30,31,37和38能够抑制JB6C141细胞系中致癌细胞核因子AP-1的转录活性,而化合物30-34,37和38对软体动物北寄贝晶杆中的1, 3-β-D-葡萄糖内切酶具有明显的抑制活性[17]。Zhuravleva等[18]从P.thomii和P.lividum两株菌株的代谢产物中进一步研究分离得到7个同类化合物Sargassopenillines A—G (40—46),其中化合物Sargassopenilline C (42)能够抑制JB6 C141细胞系中AP-1的转录活性,IC50为15 μmol/L[18]。此外,化合物Sargassopenilline D (43)和F (45)对CD-1小鼠腹腔巨噬细胞表现出细胞毒性,在10 μmol/L的安全浓度下,对细胞黏附的抑制率为30%-40%[18]。
上述化合物的结构如图 4所示。
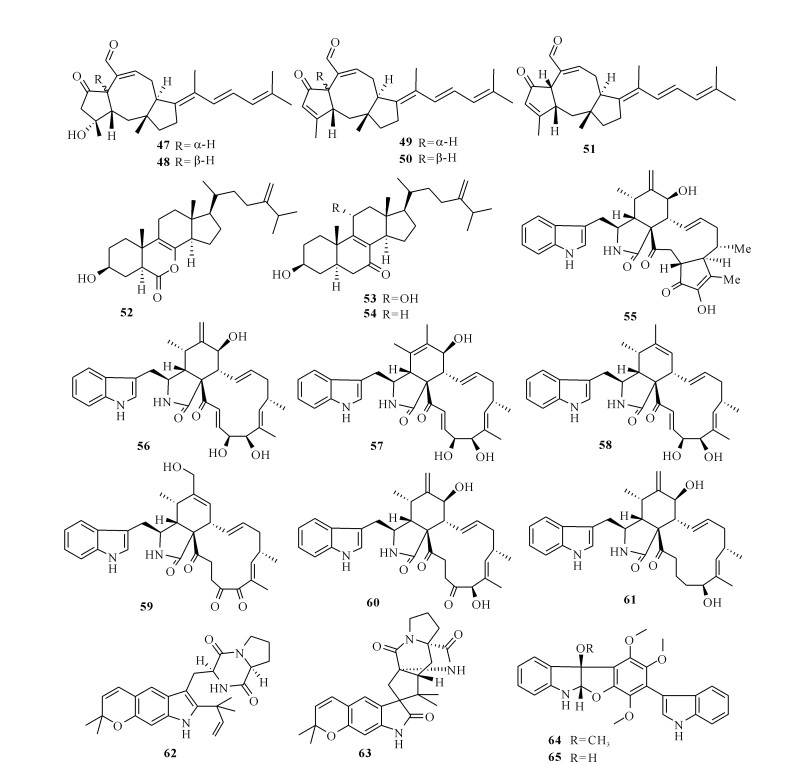
Choi等[19]从越南岘港山茶半岛的一株扇藻中分离出曲霉属真菌Aspergillus flocculosus 168ST-16.1,并从其代谢产物中分离得到5个新的Ophiobolins类二倍半萜(47-51),这些化合物对6种肿瘤细胞株HCT-15、NUGC-3、NCI-H23、ACHN、PC-3和MDA-MB-231均表现出显著的细胞毒性,半数抑制率IC50为0.14-2.01 μmol/L。这些Ophiobolins类二倍半萜对多种肿瘤细胞株的半数抑制率在纳摩尔每升级别,显示出很好的抗肿瘤药用潜力[19]。
Cui等[20]从海洋褐藻Sargassum kjellmanianum中分离得到曲霉属真菌Aspergillus ochraceus EN-31,并从其提取物中分离鉴定出1个具有罕见戊内酯B环骨架的化合物7-nor-ergosterolide (52),以及2个新的甾体衍生物53和54。化合物52对人肺癌细胞NCI-H460、肝癌细胞SMMC-7721和胰腺癌细胞SW1990表现出细胞毒性,IC50分别为5.0,7.0,28.0 μg/mL;化合物53对SMMC-7721细胞株具有细胞毒性,IC50为28.0 μg/mL[20]。Cui等[21]还从中国青岛海岸采集的绿藻Ulva pertusa中分离得到毛壳球属真菌Chaetomium globosum QEN-14,并从其代谢产物中分离得到7个新的细胞松弛素衍生物Cytoglobosins A—G (55-61)。Cytoglobosins C和D (57和58)对肺癌细胞A-549表现出细胞毒活性,IC50分别为2.26和2.55 μmol/L[21]。
Zhang等[22]从红藻中分离得到一株真菌Paecilomyces variotii EN-291,并从其发酵产物中分离得到两个异戊烯吲哚类生物碱(62和63),两种化合物具有一定的细胞毒性,对NCI-H460细胞株的IC50分别为55.9和69.3 μmol/L。此后,该团队又从此菌株中分离出2个吲哚衍生物Varioloids A和B (64和65),两化合物对人肺癌细胞A549、人结直肠癌HCT116和肝癌细胞HepG2均显示出细胞毒性,IC50为2.6—8.2 μg/mL[23]。
化合物47—65的结构如图 5所示。
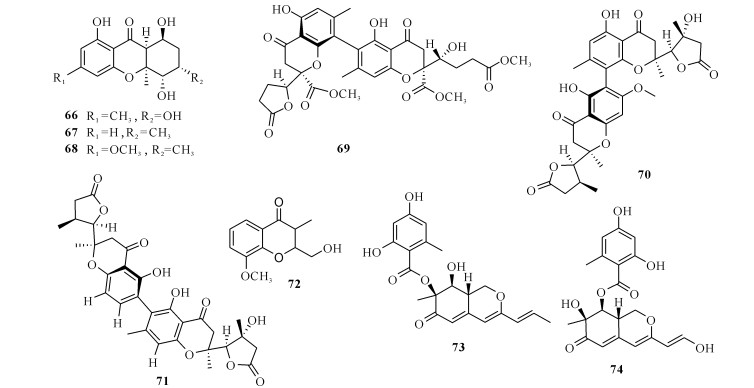
Krick等[24]从绿藻内部组织中分离得到真菌Monodictys putredinis,该菌株可产生3个新的单体氧杂蒽酮Monodictysins A—C (66—68),其中化合物67具有抑制细胞色素P450 1A活性的作用,IC50为3.0 μmol/L;化合物67和68在小鼠Hepa 1c1c7细胞中显示出适度的醌还原酶(QR)诱导活性,二倍QR活性所需浓度(CD值)分别为12.0和12.8 μmol/L;化合物68对芳香化酶具有微弱的抑制活性。
Pontius等[25]从地中海海藻共附生真菌Nodulisporium sp.代谢产物中分离得到1个新的聚酮化合物Noduliprevenone (69),该化合物可选择性抑制小鼠细胞色素P450 1A的活性(IC50为6.5 μmol/L),同时以剂量依赖的方式诱导醌还原酶(QR)的双重特异性活性,表现出潜在的抗肿瘤活性。Pontius等[26]从海藻共附生真菌Monodictys putredinis中分离出两个新颖的二聚色酮(70和71),这两个化合物能够抑制细胞色素P450 1A的活性,IC50分别为5.3和7.5 μmol/L;化合物70和71均具有适度诱导小鼠Hepa 1c1c7细胞中的NAD(P)H:醌还原酶(QR)活性的能力,IC50分别为22.1,24.8 μmol/L;化合物71在抑制芳香酶CYP19活性方面稍强于化合物70,IC50分别为24.4,16.5 μmol/L。
新色酮衍生物Chromanone A (72)分离于海藻Ulva sp.EG-5共附生青霉属真菌[27]。通过测试该化合物对致癌物代谢酶(CYP1A、GST、QR和mEH)的调节作用发现,在小鼠肝癌细胞(Hepa 1c1c7)中,化合物72 (4 μg/mL)对CYP1A的抑制率高达60%,且在低浓度时能显著诱导GST,对mEH活性的提升呈剂量依赖性;此外,化合物72具有选择性清除羟基自由基的活性,对细胞中诱导的DNA损伤有抑制作用,由此证明化合物72可能通过调节致癌物代谢酶和保护DNA免受损伤而发挥抗肿瘤作用[27]。
Myobatake等[28]从海藻衍生真菌Penicillium pinophilum Hedgcok的次级代谢产物中分离得到2个新的氢化氮杂苯甲酮化合物(73和74),两者具有选择性抑制哺乳动物DNA聚合酶A (pol γ)、B (pols α,δ和ε)和Y (pols η,ι和κ)家族的活性,其中化合物73抑制活性较强,IC50为48.6—55.6 μmol/L;动力学分析表明,化合物73是pol α和κ活性区域DNA模板引物底物的非竞争性抑制剂,而与核苷酸底物则是竞争性抑制剂。
化合物66—74的结构详见图 6。
1.3 抗氧化活性天然产物
海藻的抗氧化活性广为人知,在其共附生真菌中发现大量抗氧化活性天然产物,这提示我们海藻共附生微生物可能是其宿主海藻发挥抗氧化活性的重要因素。
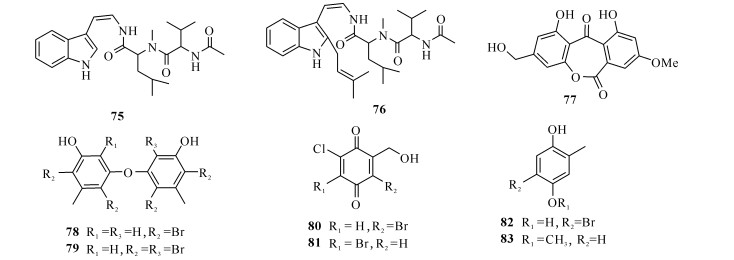
Izumikawa等[29]从日本冲绳县石垣岛采集的马尾藻中分离得到海洋真菌Aspergillus sp.SpD081030G1f1,并从其代谢产物中分离到2个新的萜素类似物JBIR-81 (75)和JBIR-82 (76),化合物75和76在神经母细胞瘤-视网膜混合细胞(N18-RE-105细胞)中,抗L-谷氨酸毒性的保护活性(半数最大效应浓度EC50分别为0.7和1.5 mmol/L)强于阳性对照抗氧化剂α-生育酚(EC50为8.8 mmol/L)。
Li等[30]使用PDB培养基对马尾藻共附生真菌Aspergillus wentii EN-48进行培养,从其代谢产物中分离得到1个新的蒽醌衍生物77,在抗氧化活性研究中表现出显著的DPPH自由基清除能力,IC50为5.2 μg/mL,明显高于阳性对照丁羟甲苯BHT (IC50为36.9 μg/mL)。
韩国釜庆大学Son小组通过向真菌培养基中加入溴化剂,陆续从不同海藻共附生真菌中分离得到一系列抗氧化活性化合物:2010年,从庆南Yogke岛采集的海洋红藻中分离出一株产黄青霉菌株(MFB574-2),通过向该菌株培养基中添加CaBr2,诱导其产生2个新的多溴联苯醚78和79,两化合物均具有DPPH自由基清除活性,IC50分别为18和15 μmol/L,活性均强于阳性对照抗坏血酸(IC50为20 μmol/L)[31];同年,向红藻共附生茎点霉属真菌Phoma herbarum MFA301的培养基中加入CaBr2,从其乙酸乙酯提取物中分离得到2个新的具有DPPH自由基清除活性的溴化龙胆醌类化合物(80和81),IC50分别为3.8和3.9 μmol/L[32];2012年,在红藻共附生真菌Dothideomycete sp.的培养基中加入NaBr,诱导其产生2个邻甲基对苯二酚类化合物(82和83),这两个化合物均具有显著的DPPH自由基清除活性,IC50分别为11.0和17.0 μmol/L[33]。
上述化合物结构如图 7所示。
1.4 抗炎活性天然产物
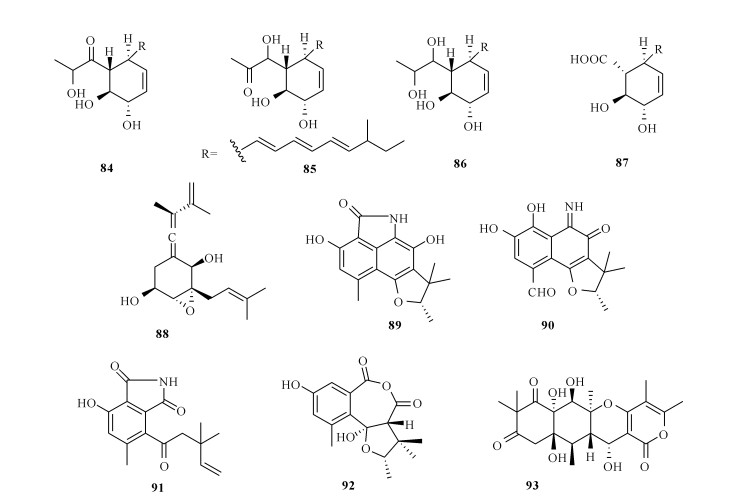
Elsebai等[34]从海藻共附生真菌Phaeosphaeria spartinae次级代谢产物中分离得到4个新的聚酮类化合物Spartinols A—D (84—87),其中化合物85对炎症中涉及的人白细胞弹性蛋白酶(HLE)具有抑制活性,IC50为17.7 μg/mL。一年后,该团队又从此菌株的发酵物中分离得到1个新化合物Spartinoxide (88),化合物88对人白细胞弹性蛋白酶具有显著的抑制活性,IC50为1.71 μg/mL[35]。2011年,该团队从海洋绿藻Enteromorpha sp.中分离得到共附生真菌Coniothyrium cereale,该菌株可代谢产生2个新的聚酮类生物碱(-)-cereolactam (89)和(-)-cereoaldomine (90),两化合物均具有选择性抑制人白细胞弹性蛋白酶的活性,IC50分别为9.28和3.01 μmol/L[36]。2012年,该团队再次从真菌Coniothyrium cereal中分离得到新的吲哚类生物碱Conioimide (91)和聚酮类化合物Cereoanhydride (92),化合物91对人白细胞弹性蛋白酶呈现出显著的选择性活性,IC50为0.2 μg/mL[37]。Wang等[38]从海藻共附生真菌Aspergillus sp.ZL0-1b14中分离出高度氧化的重排三酮倍半萜类化合物Aspertetranone D (93),在脂多糖LPS刺激的RAW264.7巨噬细胞抗炎活性实验中,表现出显著的抗炎活性,在浓度为40 μmol/L时对IL-6生成抑制率为69%。化合物84—93的结构见图 8。
目前海藻共附生真菌来源的抗炎天然产物研究较少,主要是前述两个研究团队的成果。因此,在海藻共附生真菌中抗炎天然产物的筛选发现,还有待深入研究。
1.5 浮游生物抑制活性天然产物海藻共附生真菌产生对浮游生物具有抑制活性的次级代谢产物,与抗菌活性成分类似,同样可以理解为是共附生真菌为宿主海藻提供的化学防御武器。一些海藻是珊瑚礁生物群落的重要组成部分,这些海藻共附生微生物产生的活性物质和生物信号分子,可以保护海藻的生长,从而维护珊瑚礁生态系统的平衡。
Miao等[39]向褐藻共附生曲霉属真菌Aspergillus wentii.na-3的培养基中加入异羟戊酸进行发酵,从其代谢产物中分离得到2个新的萜类化合物Aspewentins A和B (94和95):化合物94对浮游植物C.marina和H.akashiwo具有抑制作用,LC50分别为0.81,2.88 μmol/L;化合物95对海洋浮游动物卤虫藻表现出毒性作用,LC50为6.36 μmol/L。
Shi等[40]从海洋红藻Gracilaria vermiculophylla共附生真菌Trichoderma virens Y13-3中分离得到3个具有独特四环碳骨架的聚酮类化合物Trichorenins A—C (96—98),化合物96—98对两种海洋浮游植物均具有显著的抑制作用(对海洋卡盾藻半数抑制率IC50分别为0.41,0.56和0.41 μg/mL;对剧毒卡尔藻IC50分别为1.00,0.87和0.69 μg/mL)。
Liu等[41]从海洋红藻Laurencia okamurai共附生真菌Trichoderma citrinoviride A-WH-20-3代谢产物中分离得到2个新的倍半萜类化合物99和100,以及1个新的异香豆素衍生物Trichophenol A(101),化合物99对引发赤潮的海洋浮游植物剧毒卡尔藻的生长具有抑制作用,IC50为8.1 μg/mL;化合物101对海洋卡盾藻、赤潮异弯藻、东海原甲藻抑制作用较强,IC50分别4.4,9.1和5.9 μg/mL。
化合物94—101的结构如图 9所示。
1.6 其他活性天然产物
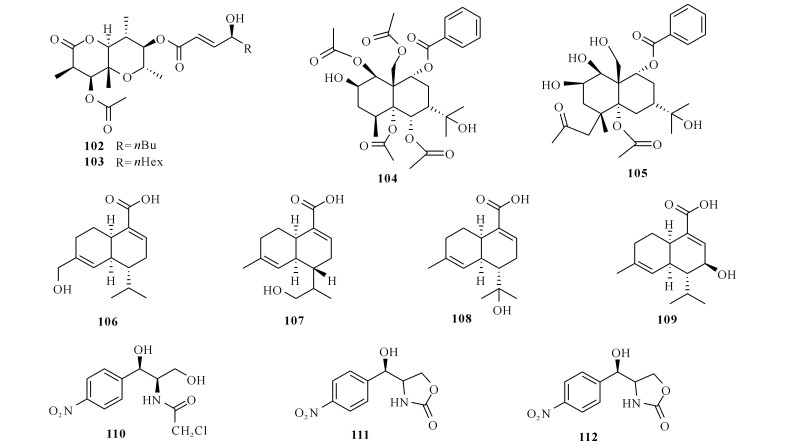
Kim等[42]从海藻共附生真菌Botryotinia sp.SF-5275中分离得到2个新化合物Botcinins A和B(102和103),化合物103对蛋白酪氨酸磷酸酶1B(PTP1B)具有显著的抑制作用,呈剂量依赖型,IC50为53.6 mmol/L;进一步研究发现,化合物103为PTP1B的非竞争性抑制剂,呈现出胰岛素拮抗活性。
Wu等[43]从红藻Sargassum horneri中分离得到真菌Pestalotiopsis sp.Z233,使用加入诱导剂CuCl2的培养基对该菌株进行培养,从其发酵物中分离得到桉烷倍半萜类化合物104和105,两个化合物均具有适度的酪氨酸酶抑制活性,IC50分别为14.8和22.3 μmol/L。
Almeida等[44]使用添加海盐的麦芽培养基对绿藻Enteromorpha sp.共附生真菌Cadophora malorum进行培养,从其提取物中分离出4个新的羟基化Sclerosporin衍生物(106—109),生物活性测定显示化合物109对3T3-L1小鼠脂肪细胞显示出较弱的脂肪堆积抑制活性(IC50为212 μmol/L)。
Chen等[45]对海藻共附生真菌Acremonium vitellinum进行化学研究,从中分离出3个氯霉素衍生物(110—112):化合物111对农业害虫棉铃虫表现出显著抑制活性,LC50为(0.56±0.03) mg/mL;化合物110和112的活性较弱,LC50分别为(0.93±0.05)mg/mL和(0.91±0.06) mg/mL;而阳性对照苦参碱的LC50仅为(0.24±0.01) mg/mL,表明化合物111具有较好的新型环保型生物农药开发前景。
化合物102—112的结构详见图 10。
2 展望
综上,海藻共附生真菌次级代谢产物中不乏含硫、氯、溴等杂原子取代的天然产物,其中萜类、聚酮类、生物碱类占据比例较大,其次为内酯、肽类、甾类化合物。海藻共附生真菌代谢产物的生物活性主要集中在抗菌和抗肿瘤领域,其次为抗氧化、抗炎等其他活性。这些活性天然产物的产生与特殊的生存环境及宿主的生长调节、化学防御等生命活动密切相关。
海藻共附生真菌活性次级代谢产物研究虽已取得一定进展,但其具体的代谢意义和特殊性,以及与藻类宿主的微妙关系仍有待深入探究。海洋蕴藏着丰富的资源,仍有大量海藻及其共附生真菌尚未开发。而研究海藻共附生真菌的多样性和分布,融合微生物学、基因组学、天然有机化学、化学生物学等多领域学科知识,将使得海藻真菌及其天然产物化学的宝贵资源得到充分有效的开发与利用。
| [1] |
JIN L M, QUAN C S, HOU X Y, et al. Potential pharmacological resources:Natural bioactive compounds from marine-derived fungi[J]. Marine Drugs, 2016, 14(4): 76. DOI:10.3390/md14040076 |
| [2] |
SURYANARAYANAN T S. Fungal endosymbionts of seaweeds[J]. Biology of Marine Fungi, 2012, 53: 53-69. |
| [3] |
JI N Y, WANG B G. Mycochemistry of marine algicol-ous fungi[J]. Fungal Diversity, 2016, 80(1): 301-342. |
| [4] |
贾铁争, 刘红兵, 方玉春, 等. 海藻真菌次级代谢产物研究进展[J]. 中国抗生素杂志, 2006, 31(6): 328-334, 345. DOI:10.3969/j.issn.1001-8689.2006.06.002 |
| [5] |
LI X D, MIAO F P, LIANG X R, et al. Meroterpenes from an algicolous strain of Penicillium echinulatum[J]. Magnetic Resonance in Chemistry, 2014, 52(5): 247-250. |
| [6] |
LIU H, LI X M, LIU Y, et al. Chermesins A-D:Meroterpenoids with a drimane-type spirosesquiterpene skeleton from the marine algal-derived endophytic fungus Penicillium chermesinum EN-480[J]. Journal of Natural Products, 2016, 79(4): 806-811. |
| [7] |
LI X, LI X M, ZHANG P, et al. A new phenolic enamide and a new meroterpenoid from marine alga-derived endophytic fungus Penicillium oxalicum EN-290[J]. Journal of Asian Natural Product Research, 2015, 17(12): 1204-1212. DOI:10.1080/10286020.2015.1117454 |
| [8] |
ZHANG P, LI X M, LI X, et al. New indole-diterpenoids from the algal-associated fungus Aspergillus nidulans[J]. Phytochemistry Letters, 2015, 12: 182-185. |
| [9] |
GAO S S, LI X M, LI C S, et al. Penicisteroids A and B, antifungal and cytotoxic polyoxygenated steroids from the marine alga-derived endophytic fungus Penicillium chrysogenum QEN-24S[J]. Bioorganic & Medicinal Chemistry Letters, 2011, 21(10): 2894-2897. |
| [10] |
SONG Y P, SHI Z Z, MIAO F P, et al. Tricholumin A, a highly transformed ergosterol derivative from the alga-endophytic fungus Trichoderma asperellum[J]. Organic Letters, 2018, 20(19): 6306-6309. DOI:10.1021/acs.orglett.8b02821 |
| [11] |
SONG Y P, LIU X H, SHI Z Z, et al. Bisabolane, cyclonerane, and harziane derivatives from the marine-alga-endophytic fungus Trichoderma asperellum cf44-2[J]. Phytochemistry, 2018, 152: 45-52. DOI:10.1016/j.phytochem.2018.04.017 |
| [12] |
ZHANG P, MANDI A, LI X M, et al. Varioxepine A, a 3H-oxepine-containing alkaloid with a new oxa-cage from the marine algal-derived endophytic fungus Paecilomyces variotii[J]. Organic Letters, 2014, 16(18): 4834-4837. DOI:10.1021/ol502329k |
| [13] |
ZHANG P, LIA X M, WANG J N, et al. Oxepine-containing diketopiperazine alkaloids from the algal-derived endophytic fungus Paecilomyces variotii EN-291[J]. Helvetica Chimica Acta, 2015, 98(6): 800-804. DOI:10.1002/hlca.201400328 |
| [14] |
DU F Y, LI X M, LI C S, et al. Cristatumins A-D, new indole alkaloids from the marine-derived endophytic fungus Eurotium cristatum EN-220[J]. Bioorganic & Medicinal Chemistry Letters, 2012, 22(14): 4650-4653. |
| [15] |
GULDER T A, HONG H, CORREA J, et al. Isolation, structure elucidation and total synthesis of lajollamide A from the marine fungus Asteromyces cruciatus[J]. Marine Drugs, 2012, 10(12): 2912-2935. DOI:10.3390/md10122912 |
| [16] |
YANG S Q, LI X M, LI X, et al. Two new diketomorpholine derivatives and a new highly conjugated ergostane-type steroid from the marine algal-derived endophytic fungus Aspergillus alabamensis EN-547[J]. Marine Drugs, 2018, 16(4): 114. DOI:10.3390/md16040114 |
| [17] |
ZHURAVLEVA O I, SOBOLEVSKAYA M P, LESH-CHENKO E V, et al. Meroterpenoids from the alga-derived fungi Penicillium thomii maire and Penicillium lividum westling[J]. Journal of Natural Products, 2014, 77(6): 1390-1395. |
| [18] |
ZHURAVLEVA O I, SOBOLEVSKAYA M P, AFIYATULLOV S, et al. Sargassopenillines A-G, 6, 6-spiroketals from the alga-derived fungi Penicillium thomii and Penicillium lividum[J]. Marine Drugs, 2014, 12(12): 5930-5943. DOI:10.3390/md12125930 |
| [19] |
CHOI B-K, TRINH P T H, LEE H-S, et al. New ophiobolin derivatives from the marine fungus Aspergillus flocculosus and their cytotoxicities against cancer cells[J]. Marine Drugs, 2019, 17(6): 346. DOI:10.3390/md17060346 |
| [20] |
CUI C M, LI X M, MENG L, et al. 7-Nor-ergosterolide, a pentalactone-containing norsteroid and related steroids from the marine-derived endophytic Aspergillus ochraceus EN-31[J]. Journal of Natural Products, 2010, 73(11): 1780-1784. DOI:10.1021/np100386q |
| [21] |
CUI C M, LI X M, LI C S, et al. Cytoglobosins A-G, cytochalasans from a marine-derived endophytic fungus, Chaetomium globosum QEN-14[J]. Journal of Natural Products, 2010, 73(4): 729-733. |
| [22] |
ZHANG P, LI X M, WANG J N, et al. Prenylated indole alkaloids from the marine-derived fungus Paecilomyces variotii[J]. Chinese Chemical Letters, 2015, 26(3): 313-316. DOI:10.1016/j.cclet.2014.11.020 |
| [23] |
ZHANG P, LI X M, MAO X X, et al. Varioloid A, a new indolyl-6, 10b-dihydro-5aH-[J]. Beilstein Journal of Organic Chemistey, 2016, 12: 2012-2018. DOI:10.3762/bjoc.12.188 |
| [24] |
KRICK A, KEHRAUS S, GERHÄUSER C, et al. Potential cancer chemopreventive in vitro activities of monomeric xanthone derivatives from the marine algicolous fungus Monodictys putredinis[J]. Journal of Natural Products, 2007, 70(3): 353-360. |
| [25] |
PONTIUS A, KRICK A, KEHRAUS S, et al. Noduliprevenone:A novel heterodimeric chromanone with cancer chemopreventive potential[J]. Chemistry-A European Journal, 2008, 14(32): 9860-9863. |
| [26] |
PONTIUS A, KRICK A, MESRY R, et al. Monodic-tyochromes A and B, dimeric xanthone derivatives from the marine algicolous fungus Monodictys putredinis[J]. Journal of Natural Products, 2008, 71(11): 1793-1799. |
| [27] |
GAMAL-ELDEEN A M, ABDEL-LATEFF A, OKINO T. Modulation of carcinogen metabolizing enzymes by chromanone A; a new chromone derivative from algicolous marine fungus Penicillium sp.[J]. Environmental Toxicology and Pharmacology, 2009, 28(3): 317-322. |
| [28] |
MYOBATAKE Y, TAKEUCHI T, KURAMOCHI K, et al. Pinophilins A and B, inhibitors of mammalian A-, B-, and Y-family DNA polymerases and human cancer cell proliferation[J]. Journal of Natural Products, 2012, 75(2): 135-141. |
| [29] |
IZUMIKAWA M, HASHIMOTO J, TAKAGI M, et al. Isolation of two new terpeptin analogs-JBIR-81 and JBIR-82 from a seaweed-derived fungus, Aspergillus sp.SpD081030G1f1[J]. The Journal of Antibiotics, 2010, 63(7): 389-391. |
| [30] |
LI X, LI X M, XU G M, et al. Antioxidant metabolites from marine alga-derived fungus Aspergillus wentii EN-48[J]. Phytochemistry Letters, 2014, 7(1): 120-123. |
| [31] |
YANG G H, YUN K, NENKEP V N, et al. Induced production of halogenated diphenyl ethers from the marine derived fungus Penicillium chrysogenum[J]. Chemistry & Biodiversity, 2010, 7(11): 2766-2770. |
| [32] |
NENKEP V N, YUN K, LI Y, et al. New production of haloquinones, bromochlorogentisylquinones A and B, by a halide salt from a marine isolate of the fungus Phoma herbarum[J]. The Journal of Antibiotics, 2010, 63(4): 199-201. |
| [33] |
LEUTOU A S, YUN K, CHOI H D, et al. New production of 5-bromotoluhydroquinone and 4-O-methyltoluhydroquinone from the marine-derived fungus Dothideomycete sp.[J]. Journal of Microbiology and Biotechnology, 2012, 22(1): 80-83. |
| [34] |
ELSEBAI M F, KEHRAUS S, GVTSCHOW M, et al. New polyketides from the marine-derived fungus Phaeosphaeria spartinae[J]. Natural Product Communications, 2009, 4(11): 1463-1468. |
| [35] |
ELSEBAI M F, KEHRAUS S, GVTSCHOW M, et al. Spartinoxide, a new enantiomer of A82775C with inhibitory activity toward HLE from the marine-derived fungus Phaeosphaeria spartinae[J]. Natural Product Communications, 2010, 5(7): 1071-1076. |
| [36] |
ELSEBAI M F, NATESAN L, KEHRAUS S, et al. HLE-inhibitory alkaloids with a polyketide skeleton from the marine-derived fungus Coniothyrium cereale[J]. Journal of Natural Products, 2011, 74(10): 2282-2285. |
| [37] |
ELSEBAI M F, NAZIR M, KEHRAUS S, et al. Polyketide skeletons from the marine alga-derived fungus Coniothyrium cereale[J]. European Journal of Organic Chemistry, 2012, 2012(31): 6197-6203. |
| [38] |
WANG Y Z, QI S, ZHAN Y, et al. Aspertetranones A-D, putative meroterpenoids from the marine algal-associated fungus Aspergillus sp.ZL0-1b14[J]. Journal of Natural Products, 2015, 78(10): 2405-2410. |
| [39] |
MIAO F P, LIANG X R, LIU X H, et al. Aspewentins A-C, norditerpenes from a cryptic pathway in an algicolous strain of Aspergillus wentii[J]. Journal of Natural Products, 2014, 77(2): 429-432. |
| [40] |
SHI Z Z, MIAO F P, FANG S T, et al. Trichorenins A-C, algicidal tetracyclic metabolites from the marine-alga-epiphytic fungus Trichoderma virens Y13-3[J]. Journal of Natural Products, 2018, 81(4): 1121-1124. |
| [41] |
LIU X H, HOU X L, SONG Y P, et al. Cyclonerane sesquiterpenes and an isocoumarin derivative from the marine-alga-endophytic fungus Trichoderma citrinoviride A-WH-20-3[J]. Fitoterapia, 2020, 141: 104469. DOI:10.1016/j.fitote.2020.104469 |
| [42] |
KIM M Y, SOHN J H, JANG J H, et al. Two new botcinin derivatives encountered in the studies of secondary metabolites from the marine-derived fungus Botryotinia sp.SF-5275[J]. The Journal of Antibiotics, 2012, 65(3): 161-164. |
| [43] |
WU B, WU X D, SUN M, et al. Two novel tyrosinase inhibitory sesquiterpenes induced by CuCl2 from a marine-derived fungus Pestalotiopsis sp.Z233[J]. Marine Drugs, 2013, 11(8): 2713-2721. |
| [44] |
ALMEIDA C, EGUEREVA E, KEHRAUS S, et al. Hydroxylated sclerosporin derivatives from the marine-derived fungus Cadophora malorum[J]. Journal of Natural Products, 2010, 73(3): 476-478. |
| [45] |
CHEN D, ZHANG P, LIU T, et al. Insecticidal activities of chloramphenicol derivatives isolated from a marine alga-derived endophytic fungus, Acremonium vitellinum, against the cotton bollworm, Helicoverpa armigera (Hubner) (Lepidoptera:Noctuidae)[J]. Molecules, 2018, 23(11): 2995. DOI:10.3390/molecules23112995 |