2. 广西国际壮医医院, 广西南宁 530200;
3. 广西中医药大学制药厂, 广西南宁 530023
2. International Zhuang Medical Hospital of Guangxi, Nanning, Guangxi, 530200, China;
3. Pharmaceutical Factory, Guangxi University of Chinese Medicine, Nanning, Guangxi, 530023, China
外感风痧颗粒由广西中医药大学百年乐制药厂生产。该方源自壮族民间验方,由苍耳草、狗仔花、山芝麻、藤苦参、岗梅、两面针等6味药制成,具有祛风清热的功效,临床用于风热感冒、咽喉肿痛。现代药理研究表明,外感风痧颗粒(片)剂对致热大鼠有解热、镇痛、消炎、抑菌、增强免疫功能的作用[1]。外感风痧颗粒的现行质量标准执行卫生部标准WS3-B-2119-96,其中只有性状项、颗粒剂检查项和生物碱、黄酮类成分的理化鉴别项,无法有效控制外感风痧颗粒的质量。外感风痧颗粒(片)是广西中医药大学百年乐制药厂的特色品种。为保障人民群众用药的安全有效性,并推广外感风痧颗粒的应用,外感风痧颗粒标准的完善势在必行,有必要增加含量测定项对其中的指标性成分进行测定。关于外感风痧颗粒的质量控制研究报道较少,罗宇东等[2]对无糖型外感风痧颗粒质量标准进行研究,使用薄层色谱法定性鉴别了藤苦参和岗梅,并采用高效液相色谱法对产品中的绿原酸进行了含量测定。中药及中药复方中所含组分较多,其功效的产生是多组分协同作用的结果,因此单一组分的质量控制已不能满足需要,近年来多数学者均选择采用多指标控制的方法[3-5]。为了更全面、客观地评价外感风痧颗粒的质量,本文拟采用多指标控制法对其进行质量控制。通过查阅相关文献[6-10],本文拟选择外感风痧颗粒中原儿茶酸、原儿茶醛、绿原酸、咖啡酸4种成分为主要监测指标并进行波长转换的HPLC法,以期为外感风痧颗粒的质量控制提供实验依据。
1 材料与方法 1.1 材料美国Waters e2695型高效液相色谱仪,四元泵,柱温箱,可变波长检测器;SQP电子分析天平(百万分之一),赛多利斯科学仪器北京有限公司;KQ5200B型超声波清洗器,昆山市超声仪器有限公司。
水为纯净水,甲醇为分析纯,乙腈为色谱纯。实验用对照品原儿茶酸(批号:110809-201205,含量:99.9%),原儿茶醛(批号:110810-201608,含量:99.3%),绿原酸(批号:110753-201817,含量:96.8%),咖啡酸(批号:110885-201703,含量:99.7%),均购自中国食品药品检定研究院。外感风痧颗粒(批号:20180304,20180401,20180402)由广西中医药大学百年乐制药厂提供。
1.2 方法 1.2.1 HPLC法色谱条件:色谱柱为依利特Hypersil C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.2%磷酸,梯度洗脱:0~5 min,8%乙腈;5~11 min,8%~12%乙腈;11~25 min,12%~21%乙腈;25~30 min,21%~25%乙腈;30~35 min,25%~100%乙腈;35~40 min,100%乙腈;进样量10 μL。柱温:25℃。流速:1.0 mL·min-1。转换波长条件:0~16 min,273 nm;16~41 min,327 nm。
本法进行系统的适用性及专属性试验,要求理论塔板数以绿原酸计应不少于3 000。
1.2.2 混合对照品溶液的制备精密称取原儿茶酸9.18 mg,置5 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照品储备溶液1;精密称取原儿茶醛6.18 mg,咖啡酸7.44 mg,置10 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照品储备溶液2;精密称取绿原酸4.6 mg,置10 mL棕色量瓶中,精密吸取对照品储备液1和储备液2各1 mL并入同一量瓶中,再加适量甲醇超声使绿原酸溶解并加甲醇稀释至刻度,摇匀,即得混合对照品储备溶液。分别精密量取0.20 mL、0.60 mL、1.00 mL、1.40 mL、1.80 mL混合对照品储备溶液,置10 mL量瓶中, 加甲醇稀释至刻度, 摇匀,即得5种不同浓度的混合对照品溶液。
1.2.3 供试品溶液的制备取外感风痧颗粒样品10袋,除去包装,精密称定,求得平均装量,然后取样品适量,研细,取约10.0 g,精密称定,置锥形瓶中,精密加入甲醇25 mL,密塞,称定质量后,超声40 min,放冷,再称定质量,并用甲醇补足减失的质量,摇匀,静置,将上清液滤过,取续滤液,即得供试品溶液。
2 结果与分析 2.1 样品测定取3批外感风痧颗粒样品,分别按1.2.3节方法制备供试品溶液,在1.2.1节色谱条件下记录色谱图并用标准曲线法计算原儿茶酸、原儿茶醛、绿原酸、咖啡酸的含量,结合平均装量计算每袋(标示装量15 g)中所含指标成分的质量(mg),结果见表 1。
| 批号 Lot number | 含量Content(mg·袋-1) | |||
| 原儿茶酸 Protocatechuic acid | 原儿茶醛 Protocatechuic aldehyde | 绿原酸 Chlorogenic acid | 咖啡酸 Caffeic acid | |
| 20180304 | 0.69 | 0.30 | 1.6 | 0.20 |
| 20180401 | 0.62 | 0.30 | 1.5 | 0.22 |
| 20180402 | 0.60 | 0.26 | 1.4 | 0.21 |
2.2 系统适用性、专属性试验结果
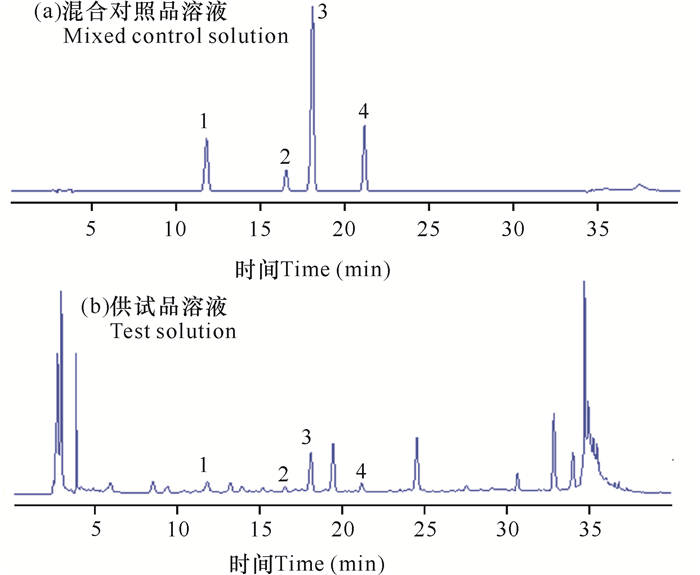
精密吸取1.2.2节和1.2.3节的混合对照品溶液、外感风痧颗粒供试品溶液,按1.2.1节色谱条件进样测定分析,考察系统适用性。结果显示,对照品色谱图和供试品色谱图的相应位置具有相同保留时间的色谱峰,经DAD检测器检测其UV光谱一致,各组分色谱峰分离度均达到1.5以上,符合含量测定的要求。典型色谱图见图 1。
|
| 1:原儿茶酸 Protocatechuic acid,2:原儿茶醛 Protocatechuic aldehyde,3:绿原酸 Chlorogenic acid,4:咖啡酸 Caffeic acid 图 1 外感风痧颗粒HPLC色谱图 Fig. 1 HPLC chromatograms of Waiganfengsha Granule |
2.3 线性关系考察
将1.2.2节5个不同浓度的混合对照品溶液注入高效液相色谱仪,进样量10 μL,测定峰面积,并以峰面积值(Y)对含量(X)(μg/mL)进行回归,分别计算4种指标的线性关系标准曲线方程,计算结果见表 2。
| 成分 Ingredient | 回归方程 Regression equation | r值 r value | 线性范围 Linear range (μg·mL-1) |
| 原儿茶酸 Protocatechuic acid | Y=19156X+1665.5 | 0.999 9 | 3.672~33.048 |
| 原儿茶醛 Protocatechuic aldehyde | Y=36902X-337.75 | 0.999 9 | 1.236~11.124 |
| 绿原酸 Chlorogenic acid | Y=25771X+18700 | 0.999 9 | 9.200~82.800 |
| 咖啡酸 Caffeic acid | Y=49419X+2206.9 | 0.999 9 | 1.488~13.392 |
2.4 精密度实验
精密吸取第3个浓度的混合对照品溶液10 μL,重复进样6次,记录色谱图,测得原儿茶酸、原儿茶醛、绿原酸、咖啡酸峰面积值,并计算峰面积的RSD值,分别为1.1%、1.0%、1.1%、1.1%, 表明仪器精密度良好。
2.5 重复性实验取6份批号为20180402的样品,分别按1.2.3节方法制备供试品溶液,精密吸取10 μL,依法测定并记录色谱图,计算得原儿茶酸、原儿茶醛、绿原酸、咖啡酸平均含量分别为0.04 mg/g、0.017 mg/g、0.090 mg/g、0.014 mg/g,RSD值分别为1.4%、1.2%、0.89%、1.6%,与2.4节的精密度实验结果基本一致,表明HPLC法及设定的色谱条件参数重复性良好。
2.6 稳定性实验取2.5节第一份供试品溶液,在0 h、2 h、4 h、8 h、12 h、24 h不同时间间隔点精密吸取10 μL进行分析,计算得原儿茶酸、原儿茶醛、绿原酸、咖啡酸峰面积的RSD值分别为1.2%、1.4%、1.7%、1.9%,表明样品在24 h内稳定。
2.7 加样回收率实验取批号为20180402的样品,研细,取约5.0 g,精密称定,平行称取6份,按照样品已知含量100%的水平加入混合对照品溶液,按1.2.3节方法制备供试品溶液,精密吸取10 μL,依法进样,计算回收率。结果:原儿茶酸、原儿茶醛、绿原酸、咖啡酸的平均回收率分别为97.6%、100.9%、100.5%、103.3%,RSD值分别为2.1%、2.8%、1.9%、2.6%,表明本文设定的HPLC方法准确度良好。具体结果见表 3。
| 成分 Ingredient | 样品中含量 Sample content (m/mg) | 加入量 Added amount (m/mg) | 测得量 Measured amount (m/mg) | 平均回 收率 Average recovery rate(%) | RSD (%) |
| 原儿茶酸 Protocatechuic acid | 0.200 | 0.180 | 0.370 | 97.6 | 2.1 |
| 原儿茶醛 Protocatechuic aldehyde | 0.085 | 0.093 | 1.175 | 100.9 | 2.8 |
| 绿原酸 Chlorogenic acid | 0.450 | 0.480 | 0.960 | 100.5 | 1.9 |
| 咖啡酸 Caffeic acid | 0.071 | 0.061 | 0.134 | 103.3 | 2.6 |
2.8 处方中个味药材的检测
分别取苍耳草、狗仔花、山芝麻、藤苦参、岗梅、两面针药材粗粉约10 g,精密称定,分别按1.2.3节方法制备供试品溶液,并采用1.2.1节色谱条件记录色谱图。通过色谱峰检识发现,除岗梅外其他各味药都含有原儿茶酸;除山芝麻外,其他各味药都含有绿原酸;狗仔花、藤苦参和山芝麻中含有原儿茶醛;狗仔花、藤苦参、山芝麻和苍耳草中均含有咖啡酸。
3 结论通过对处方中各味药材的检测可以得知,原儿茶酸、原儿茶醛、绿原酸、咖啡酸这4种组分广泛分布于苍耳草、狗仔花、山芝麻、藤苦参、岗梅、两面针这6味药材中,本文选择此4种组分作为检测指标,能够较为全面地体现投料药材的质量,有效地监控制剂的质量。
本研究通过对原药材的分析以及对提取条件、提取时间、液相条件等条件的优化,最终建立了HPLC测定外感风痧颗粒中4种指标性成分的方法,该方法简便易操作,结果准确可靠,可用于外感风痧颗粒的质量控制。
| [1] |
林启云, 李爱媛, 周芳, 等. 外感风痧颗粒(片)剂药理研究[J]. 广西中医学院学报, 2001(4): 88-90. DOI:10.3969/j.issn.1008-7486.2001.04.053 |
| [2] |
罗宇东, 陆施衡, 谭安蔷. 无糖型外感风痧颗粒质量标准的研究[J]. 中国当代医药, 2017, 24(25): 125-129. DOI:10.3969/j.issn.1674-4721.2017.25.040 |
| [3] |
郭倩, 田成旺, 朱月信, 等. HPLC法同时测定疏风解毒胶囊中7种活性成分[J]. 中草药, 2015, 46(8): 1174-1177. |
| [4] |
陈晓虎, 苏晶, 王慧, 等. UPLC法同时测定栀子金花丸中11种成分[J]. 中草药, 2014, 45(7): 955-959. |
| [5] |
王丽萍, 曹英杰, 段晓颖. HPLC同步测定润肠通丸中9种成分的含量[J]. 中国实验方剂学杂志, 2015, 21(23): 50-54. |
| [6] |
刘娟秀, 罗益远, 刘训红, 等. 不同采收期苍耳草中酚酸类及蒽醌类成分的动态积累分析[J]. 中草药, 2016, 47(7): 1204-1209. |
| [7] |
刘佳, 古炳明, 成佳玲. 山芝麻质量标准研究[J]. 中国药品标准, 2016, 17(3): 171-174. |
| [8] |
孙科, 陈冉, 陆世惠. 双波长HPLC法同时测定两面针药材中5种成分的含量[J]. 中国药房, 2017, 28(3): 393-396. |
| [9] |
杜冰曌, 杨鑫瑶, 冯晓. 岗梅的化学成分和药理作用研究进展[J]. 中国中药杂志, 2017, 42(1): 20-28. |
| [10] |
汤玉妹. 两面针化学成分的研究[J]. 中草药, 1994, 25(10): 550-550. DOI:10.3321/j.issn:0253-2670.1994.10.017 |



